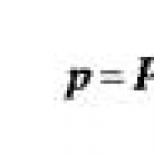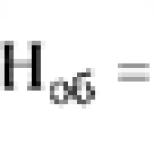Zmeny extracelulárnej koncentrácie draslíka (K). Podmienky pre vznik pokojového membránového potenciálu Šírenie vzruchu pozdĺž axónu
Myšlienku dvoch foriem konvertibilnej energie som vyjadril v roku 1975. O dva roky neskôr tento názor podporil aj Mitchell. Medzitým v skupine A. Glagoleva začali experimenty testovať jednu z predpovedí tohto nového konceptu.
Zdôvodnil som to nasledovne. Ak je protónový potenciál vyjednávacím čipom, potom musí mať bunka dostatočné množstvo takýchto „bankoviek“.
Táto požiadavka bola splnená, keď išlo o ATP. Bunka vždy obsahuje pomerne veľké množstvá ATP a boli prijaté opatrenia na stabilizáciu tohto množstva v podmienkach meniacej sa konjunktúry – neustále sa meniace rýchlosti tvorby a využitia ATP. Existuje špeciálna látka - kreatínfosfát, ktorý sa podieľa iba na jednej reakcii - fosforylácii ADP:
ADP + kreatínfosfát ⇔ ATP + kreatín.
Keď je ATP nadbytok a ADP nedostatok, reakcia prebieha sprava doľava a hromadí sa kreatínfosfát, ktorý je za týchto podmienok oveľa väčší ako ATP. Ale akonáhle hladina ADP stúpa a ATP klesá, reakcia mení smer a kreatínfosfát sa stáva dodávateľom ATP. Kreatínfosfát teda plní svoju funkciu stabilizátora, tlmivého roztoku na úrovni ATP.
A čo protónový potenciál?
Jednoduchý výpočet umožňuje previesť jednu energetickú „menu“ na druhú. Tento výpočet ukazuje, že množstvo energie akumulovanej napríklad bakteriálnou bunkou vo forme protónového potenciálu je takmer tisíckrát menšie ako množstvo ATP, ak je protónový potenciál v elektrickej forme. Toto množstvo je rovnakého rádu ako počet potenciálnych generátorov a spotrebiteľov v bakteriálnej membráne.
Táto situácia vytvára špeciálnu potrebu pufrovacieho systému, ktorý stabilizuje úroveň protónového potenciálu. V opačnom prípade aj krátkodobé prevýšenie celkovej rýchlosti procesov spotrebúvajúcich potenciál nad rýchlosťou jeho tvorby povedie k zániku potenciálu a odstaveniu všetkých systémov napájaných potenciálom.
Takže musí existovať tlmivý roztok pre protónový potenciál, ako je kreatínfosfát pre ATP. Aký komponent si však príroda vybrala do takejto úlohy?
Pri premýšľaní o tomto probléme som sa snažil nájsť nejaký potenciálny biologický systém, ktorého funkcia by bola neznáma.
Jedna zo starých záhad biológie: prečo bunka absorbuje draselné ióny a vylučuje sodíkové ióny, čím vzniká nákladná asymetria v distribúcii týchto podobných iónov medzi cytoplazmou a prostredím? Prakticky v každej živej bunke je oveľa viac iónov draslíka ako iónov sodíka, zatiaľ čo v prostredí je sodík nad draslíkom v obrovskom prebytku. Možno je Na + jed pre bunku?
Nie, nie je. Zatiaľ čo niektoré enzýmové systémy fungujú lepšie v KCl ako v NaCl, zdá sa, že ide o sekundárnu adaptáciu na vnútorné prostredie bunky s „vysokým obsahom draslíka“ a „nízkym obsahom sodíka“. Počas obrovského obdobia biologickej evolúcie sa bunka mohla prispôsobiť prirodzenému pomeru iónov alkalických kovov vo vonkajšom prostredí. Halofilné baktérie žijú v nasýtenom roztoku NaCl a koncentrácia Na + v ich cytoplazme niekedy dosahuje mol na liter, čo je takmer tisíckrát viac ako koncentrácia Na + v bežných bunkách. Takže Na+ nie je jed.
Všimnite si, že tie isté halofilné baktérie si udržujú intracelulárnu koncentráciu K+ asi 4 móly na liter, pričom míňajú obrovské množstvo energetických zdrojov na vytvorenie gradientu sodíka a draslíka.
Je známe, že excitabilné živočíšne bunky, ako sú neuróny, využívajú gradient sodíka a draslíka na vedenie nervových impulzov. Ale čo iné typy buniek, napríklad baktérie?
Prejdime k mechanizmu transportu K + a Na + cez bakteriálnu membránu. Je známe, že medzi bakteriálnou cytoplazmou a vonkajším prostredím existuje rozdiel v elektrických potenciáloch, podporovaný prácou generátorových proteínov v bakteriálnej membráne. Pumpovaním protónov z vnútra bunky von, generátorové proteíny tým negatívne nabíjajú vnútro baktérie. Za týchto podmienok by akumulácia iónov K + vo vnútri bunky mohla nastať jednoducho v dôsledku elektroforézy - pohybu kladne nabitého iónu draslíka do záporne nabitej cytoplazmy baktérie.
V tomto prípade by tok draslíka mal vybiť membránu predbežne nabitú protónovými generátormi.
Na druhej strane by vybitie membrány malo okamžite aktivovať prevádzku generátorov.
To znamená, že energetické zdroje vynaložené na generovanie rozdielu v elektrických potenciáloch medzi bunkou a prostredím sa použijú na koncentráciu K+ iónov vo vnútri bunky. Konečnou rovnováhou takéhoto procesu bude výmena intracelulárnych iónov H + za extracelulárne ióny K + (ióny H + sú odčerpávané generátorovými proteínmi, ióny K + vstupujú dovnútra a pohybujú sa v elektrickom poli vytvorenom pohybom H + ióny).
Vo vnútri bunky sa teda nevytvorí len nadbytok K + iónov, ale aj nedostatok H + iónov.
Tento deficit možno využiť na odčerpanie iónov Na +. Dá sa to urobiť nasledujúcim spôsobom. Je známe, že baktérie majú špeciálny nosič sodíkových iónov, ktorý vymieňa Na + za H + (tento nosič sa nazýva Na + /H + -antiporter). V podmienkach nedostatku H+ v cytoplazme môže antiport kompenzovať nedostatok protónov prenosom H+ z vonkajšieho prostredia do bunky. Transportér môže vyrobiť takýto antiport iba jedným spôsobom: výmenou vonkajšieho za vnútorný Na +. To znamená, že pohyb iónov H + do bunky možno využiť na odčerpanie iónov Na + z tej istej bunky.
Vytvorili sme teda gradient draslíka a sodíka: akumulovali sme K + vo vnútri bunky a odčerpávali sme odtiaľ Na +. Hnacou silou týchto procesov bol protónový potenciál vytvorený generátorovými proteínmi. (Smer potenciálu bol taký, že vnútro článku bolo nabité záporne a bol nedostatok vodíkových iónov.)
Predpokladajme teraz, že protónové generátory boli z nejakého dôvodu vypnuté. Čo sa stane s gradientom draslíka a sodíka za týchto nových podmienok?
Samozrejme, že sa rozplynie: ióny K + vytečú z bunky do okolia, kde ich je málo, ióny Na + sa dostanú dovnútra, kde je týchto iónov nedostatok.
Ale tu je to, čo je zaujímavé. Rozptyl, samotný gradient draslíka a sodíka sa ukáže ako generátor protónového potenciálu rovnakého smeru, ktorý sa vytvoril počas prevádzky proteínových generátorov.
Uvoľnenie iónu K + ako kladne nabitej častice skutočne vytvára rozdiel difúzneho potenciálu na bunkovej membráne so znamienkom mínus vo vnútri bunky. Vstup Na + za účasti Na + /H + - antiportera bude sprevádzaný uvoľnením H +, to znamená vytvorením nedostatku H + vo vnútri bunky.
tak čo sa stane? Keď fungujú generátory proteínov, protónový potenciál, ktorý vytvárajú, sa vynakladá na tvorbu gradientu draslíka a sodíka. Ale keď sú vypnuté (alebo ich výkon nestačí na uspokojenie mnohých spotrebiteľov potenciálu), gradient draslíka a sodíka, ktorý sa rozptýli, sám začne generovať protónový potenciál.
Koniec koncov, toto je vyrovnávacia pamäť protónového potenciálu, práve vyrovnávacia pamäť, ktorá je taká potrebná pre fungovanie membránových energetických systémov!
Schematicky možno tento koncept znázorniť takto:
Draslík-sodný gradient ↓ vonkajšie zdroje energie → protónový potenciál → prac.
Ale ak je takáto schéma správna, potom by gradient draslíka a sodíka mal predĺžiť výkon bunky v podmienkach, keď sú energetické zdroje vyčerpané.
A. Glagolev a I. Brown overili platnosť tohto záveru. Bol odobratý mutant Escherichia coli bez protónovej ATP syntetázy. Pre takéhoto mutanta je oxidácia substrátov kyslíkom jediným zdrojom energie vhodným na vytvorenie protónového potenciálu. Ako vtedy ukázal J. Adler a jeho spolupracovníci, mutant je mobilný, pokiaľ je v médiu kyslík.
Glagolev a Brown zopakovali Adlerov experiment a presvedčili sa, že vyčerpanie zásob kyslíka v roztoku v skutočnosti zastaví baktérie, ak sú v médiu s KCl. Za týchto podmienok neexistuje gradient draslík-sodík: v bunkách aj v prostredí je veľa draslíka a sodík nie je ani tam, ani tu.
Teraz vezmeme médium s NaCl. Za takýchto podmienok by mali existovať oba gradienty, ktoré nás zaujímajú: draslík (veľa draslíka vo vnútri a málo vonku) a sodík (veľa sodíka vonku a málo vo vnútri). Hypotéza predpovedala, že v takejto situácii bude mobilita nejaký čas pretrvávať aj v anoxických podmienkach, pretože je možná premena energie:
gradient draslík-sodík → protónový potenciál → rotácia bičíka.
V skutočnosti sa baktérie pohybovali ďalších 15-20 minút po tom, čo meracie zariadenie zaregistrovalo nulovú hladinu CO v médiu.
Ale obzvlášť pozoruhodný, ako by sa dalo očakávať, bol experiment s baktériami milujúcimi soľ, ktoré transportujú veľmi veľké množstvo iónov K + a Na +, aby vytvorili gradient draslíka a sodíka. Takéto baktérie sa rýchlo zastavili v tme za anoxických podmienok, ak bol v médiu KCl, a stále sa pohybovali po deviatich (!) hodinách, ak bol KCl nahradený NaCl.
Táto hodnota – deväť hodín – je zaujímavá predovšetkým ako ilustrácia objemu energetického rezervoára, ktorým je gradient draslíka a sodíka u slanomilných baktérií. Okrem toho nadobúda osobitný význam, ak si spomenieme, že baktérie milujúce soľ majú bakteriorhodopsín, a preto sú schopné premieňať svetelnú energiu na protónový potenciál. Je jasné, že takáto premena je možná len počas denného svetla. A čo v noci? Ukazuje sa teda, že energia uložená počas dňa vo forme gradientu draslíka a sodíka vystačí na celú noc.
Konštatovanie, že gradient draslíka a sodíka zohráva úlohu tlmivého roztoku protónového potenciálu, nám umožňuje pochopiť nielen biologickú funkciu tohto gradientu, ale aj dôvod, ktorý dlhé roky bránil objasneniu jeho významu pre život bunky. Myšlienka vyrovnávacej úlohy gradientu draslíka a sodíka sa nemohla zrodiť skôr, ako bol objavený protónový potenciál a bolo dokázané, že slúži ako konvertibilná forma energie. Celé tie roky problém draslíka a sodíka len čakal v krídlach.
Existujú teda dve skutočnosti, ktoré je potrebné vziať do úvahy, aby sme pochopili mechanizmy, ktoré udržiavajú pokojový membránový potenciál.
1 . Koncentrácia draselných iónov v bunke je oveľa vyššia ako v extracelulárnom prostredí. 2 . Membrána v pokoji je selektívne permeabilná pre K + a pre Na + je permeabilita membrány v pokoji zanedbateľná. Ak vezmeme priepustnosť draslíka ako 1, potom priepustnosť sodíka v pokoji bude len 0,04. teda dochádza k konštantnému toku iónov K + z cytoplazmy pozdĺž koncentračného gradientu. Draslíkový prúd z cytoplazmy vytvára relatívny deficit kladných nábojov na vnútornom povrchu, pre anióny je bunková membrána nepriepustná, následkom čoho sa cytoplazma bunky nabije negatívne vzhľadom na prostredie obklopujúce bunku. Tento potenciálny rozdiel medzi bunkou a extracelulárnym priestorom, polarizácia bunky, sa nazýva pokojový membránový potenciál (RMP).
Vynára sa otázka: prečo prúd iónov draslíka nepokračuje, kým sa koncentrácie iónov mimo a vnútri bunky nevyrovnajú? Malo by sa pamätať na to, že ide o nabitú časticu, preto jej pohyb závisí aj od náboja membrány. Vnútrobunkový negatívny náboj, ktorý vzniká prúdom iónov draslíka z bunky, bráni novým iónom draslíka opustiť bunku. Tok draselných iónov sa zastaví, keď pôsobenie elektrického poľa kompenzuje pohyb iónu pozdĺž koncentračného gradientu. Preto pri danom rozdiele koncentrácií iónov na membráne vzniká pre draslík takzvaný ROVNOVÁHA POTENCIÁL. Tento potenciál (Ek) sa rovná RT/nF *ln /, (n je valencia iónu.) alebo
Ek=61,5 log/
Membránový potenciál (MP) do značnej miery závisí od rovnovážneho potenciálu draslíka, avšak časť sodíkových iónov stále preniká do pokojovej bunky, ako aj chloridové ióny. Záporný náboj, ktorý má bunková membrána, teda závisí od rovnovážnych potenciálov sodíka, draslíka a chlóru a je opísaný Nernstovou rovnicou. Prítomnosť tohto pokojového membránového potenciálu je mimoriadne dôležitá, pretože určuje schopnosť bunky excitovať – špecifickú odpoveď na podnet.
bunková excitácia
AT vzrušenie buniek (prechod z pokoja do aktívneho stavu) nastáva so zvýšením permeability iónových kanálov pre sodík a niekedy aj pre vápnik. Dôvodom zmeny permeability môže byť aj zmena potenciálu membrány - aktivujú sa elektricky excitovateľné kanály a interakcia membránových receptorov s biologicky účinná látka– receptorom riadené kanály a mechanický vplyv. V každom prípade pre rozvoj vzrušenia je to nevyhnutné počiatočná depolarizácia - mierny pokles záporného náboja membrány, spôsobené pôsobením podnetu. Dráždivou látkou môže byť akákoľvek zmena parametrov vonkajšieho alebo vnútorného prostredia tela: svetlo, teplota, chemických látok(vplyv na chuťové a čuchové receptory), naťahovanie, tlak. Sodík prúdi do bunky, dochádza k iónovému prúdu a membránový potenciál klesá - depolarizácia membrány.
Tabuľka 4
Zmena membránového potenciálu počas bunkovej excitácie.
Venujte pozornosť skutočnosti, že sodík vstupuje do bunky pozdĺž koncentračného gradientu a pozdĺž elektrického gradientu: koncentrácia sodíka v bunke je 10-krát nižšia ako v extracelulárnom prostredí a náboj vo vzťahu k extracelulárnemu je negatívny. Súčasne sú aktivované aj draslíkové kanály, ale sodíkové (rýchle) sú aktivované a inaktivované v priebehu 1–1,5 milisekúnd a draslíkové kanály trvajú dlhšie.
Zmeny membránového potenciálu sú zvyčajne znázornené graficky. Horný obrázok znázorňuje počiatočnú depolarizáciu membrány – zmenu potenciálu v reakcii na pôsobenie stimulu. Pre každú excitabilnú bunku existuje špeciálna úroveň membránového potenciálu, po dosiahnutí ktorej sa vlastnosti sodíkových kanálov dramaticky menia. Tento potenciál je tzv kritická úroveň depolarizácie (KUD). Keď sa membránový potenciál zmení na KUD, otvoria sa rýchle, na potenciáli závislé sodíkové kanály, tok sodíkových iónov sa ponáhľa do bunky. S prechodom kladne nabitých iónov do bunky v cytoplazme sa kladný náboj zvyšuje. V dôsledku toho sa transmembránový potenciálny rozdiel znižuje, hodnota MP sa znižuje na 0 a potom, keď sodík ďalej vstupuje do bunky, membrána sa znovu nabije a náboj sa obráti (prestrelí) - teraz sa povrch stáva elektronegatívnym vzhľadom na cytoplazmu - membrána je úplne DEPOLARIZOVANÁ - stredná postava. Nedochádza k ďalšej zmene poplatkov, pretože sodíkové kanály sú inaktivované- viac sodíka nemôže vstúpiť do bunky, hoci koncentračný gradient sa mení veľmi mierne. Ak má stimul takú silu, že depolarizuje membránu na FCD, tento stimul sa nazýva prahový stimul, spôsobuje excitáciu bunky. Potenciálny bod zvratu je znakom toho, že celý rozsah podnetov akejkoľvek modality bol preložený do jazyka nervového systému – excitačné impulzy. Impulzy alebo excitačné potenciály sa nazývajú akčné potenciály. Akčný potenciál (AP) – rýchla zmena membránového potenciálu v reakcii na pôsobenie prahového stimulu. AP má štandardné parametre amplitúdy a času, ktoré nezávisia od sily stimulu – pravidlo „ALL OR NIČ“. Ďalšou fázou je obnovenie pokojového membránového potenciálu - repolarizácia(dolný obrázok) je spôsobený hlavne aktívnym transportom iónov. Najdôležitejším procesom aktívneho transportu je činnosť Na/K pumpy, ktorá pumpuje sodíkové ióny von z bunky a súčasne pumpuje draselné ióny do bunky. Obnovenie membránového potenciálu nastáva v dôsledku prúdu draslíkových iónov z bunky - aktivujú sa draslíkové kanály a umožňujú draslíkovým iónom prechádzať, kým sa nedosiahne rovnovážny draslíkový potenciál. Tento proces je dôležitý, pretože kým sa MPP neobnoví, bunka nie je schopná vnímať nový excitačný impulz.
HYPERPOLARIZÁCIA - krátkodobé zvýšenie MP po jej obnovení, čo je spôsobené zvýšením priepustnosti membrány pre ióny draslíka a chlóru. Hyperpolarizácia nastáva až po PD a nie je charakteristická pre všetky bunky. Skúsme ešte raz graficky znázorniť fázy akčného potenciálu a iónové procesy, ktoré sú základom zmien membránového potenciálu (obr. 9). Na osi x vynesme hodnoty membránového potenciálu v milivoltoch a na zvislú os čas v milisekundách.
1. Depolarizácia membrány na KUD - môžu sa otvoriť akékoľvek sodíkové kanály, niekedy vápnikové, rýchle aj pomalé, závislé od napätia a riadené receptormi. Závisí to od typu stimulu a typu bunky.
2. Rýchly vstup sodíka do bunky - rýchle, napäťovo závislé sodíkové kanály sa otvárajú a depolarizácia dosiahne bod obratu potenciálu - membrána sa znovu nabije, znamienko náboja sa zmení na kladné.
3. Obnova koncentračného gradientu draslíka - prevádzka čerpadla. Draslíkové kanály sú aktivované, draslík prechádza z bunky do extracelulárneho prostredia - začína sa repolarizácia, obnova MPP
4. Stopová depolarizácia alebo negatívny stopový potenciál – membrána je stále depolarizovaná vzhľadom na MPP.
5. Hyperpolarizácia stopy. Draslíkové kanály zostávajú otvorené a dodatočný draslíkový prúd hyperpolarizuje membránu. Potom sa bunka vráti na počiatočnú úroveň MPP. Trvanie AP je pre rôzne bunky od 1 do 3-4 ms.

Obrázok 9 Fázy akčného potenciálu
Všimnite si tri potenciálne hodnoty, ktoré sú dôležité a konštantné pre každú bunku jej elektrických charakteristík.
1. MPP - elektronegativita bunkovej membrány v pokoji, poskytujúca schopnosť excitácie - excitabilita. Na obrázku MPP \u003d -90 mV.
2. KUD - kritická úroveň depolarizácie (alebo prah pre generovanie membránového akčného potenciálu) - je to hodnota membránového potenciálu, pri ktorej sa otvoria rýchlo, potenciálne závislé sodíkové kanály a membrána sa znovu nabije v dôsledku vstupu kladných sodíkových iónov do bunky. Čím vyššia je elektronegativita membrány, tým je ťažšie ju depolarizovať na FCD, tým je takýto článok menej excitabilný.
3. Potenciálny bod zvratu (prekmit) - taká hodnota pozitívne membránový potenciál, pri ktorom kladne nabité ióny už neprenikajú do bunky – krátkodobý rovnovážny sodíkový potenciál. Na obrázku + 30 mV. Celková zmena membránového potenciálu z –90 na +30 bude pre danú bunku 120 mV, táto hodnota je akčný potenciál. Ak tento potenciál vznikol v neuróne, rozšíri sa pozdĺž nervového vlákna, ak sa vo svalových bunkách rozšíri po membráne svalového vlákna a povedie ku kontrakcii, v žľazovom k sekrécii – k pôsobeniu bunky. Toto je špecifická odpoveď bunky na pôsobenie stimulu, excitácia.
Pri vystavení podnetu podprahová pevnosť dochádza k neúplnej depolarizácii - LOCAL RESPONSE (LO). Neúplná alebo čiastočná depolarizácia je zmena v náboji membrány, ktorá nedosahuje kritickú úroveň depolarizácie (CDL).
Plnenie jeho hlavných funkcií - generovania, vedenia a prenosu nervového impulzu neurónom je možné predovšetkým preto, že koncentrácia množstva iónov vo vnútri a mimo bunky sa výrazne líši. Najvyššia hodnota tu majú ióny K+, Na+, Ca2+, Cl-. V bunke je 30-40-krát viac draslíka ako vonku a asi 10-krát menej sodíka. Okrem toho je v bunke oveľa menej chloridových a voľných iónov vápnika ako v medzibunkovom médiu.
Rozdiel medzi koncentráciami sodíka a draslíka vzniká špeciálnym biochemickým mechanizmom tzv sodno-draselná pumpa. Je to molekula proteínu uložená v membráne neurónu (obr. 6) a vykonávajúca aktívny transport iónov. Takáto pumpa pomocou energie ATP (kyselina adenozíntrifosforečná) vymieňa sodík za draslík v pomere 3 : 2. Na prenos troch iónov sodíka z bunky do prostredia a dvoch iónov draslíka v opačnom smere (t.j. proti koncentrácii gradient), je potrebná energia jednej molekuly ATP.
Keď neuróny dozrievajú, v ich membráne sú zabudované sodno-draselné pumpy (na 1 μm2 môže byť umiestnených až 200 takýchto molekúl), po ktorých sa draselné ióny čerpajú do nervovej bunky a ióny sodíka sa z nej odstraňujú. V dôsledku toho sa koncentrácia iónov draslíka v bunke zvyšuje a sodík klesá. Rýchlosť tohto procesu môže byť veľmi vysoká: až 600 iónov Na+ za sekundu. V skutočných neurónoch je určená predovšetkým dostupnosťou intracelulárneho Na + a prudko sa zvyšuje s jeho prienikom zvonku. V neprítomnosti jedného z dvoch typov iónov sa činnosť pumpy zastaví, pretože môže prebiehať len ako proces výmeny intracelulárneho Na+ za extracelulárny K+.
Podobné transportné systémy existujú aj pre ióny Cl- a Ca2+. V tomto prípade sú chloridové ióny odstránené z cytoplazmy do medzibunkového prostredia a ióny vápnika sú zvyčajne prenesené do bunkových organel - mitochondrií a kanálov endoplazmatického retikula.
Na pochopenie procesov prebiehajúcich v neuróne je potrebné vedieť, že v bunkovej membráne sú iónové kanály, ktorých počet je daný geneticky. iónový kanál je diera v špeciálnej molekule proteínu uloženej v membráne. Proteín môže zmeniť svoju konformáciu (priestorovú konfiguráciu), v dôsledku čoho je kanál v otvorenom alebo uzavretom stave. Existujú tri hlavné typy takýchto kanálov:
- trvalo otvorené;
- potenciálne závislé (napäťovo závislé, elektrosenzitívne) - kanál sa otvára a zatvára v závislosti od transmembránového rozdielu potenciálov, t.j. potenciálny rozdiel medzi vonkajším a vnútorným povrchom cytoplazmatickej membrány;
- chemo-dependentný (ligand-dependentný, chemosenzitívny) - kanál sa otvára v závislosti od vplyvu jednej alebo druhej látky špecifickej pre každý kanál naň.
Mikroelektródová technika sa používa na štúdium elektrických procesov v nervovej bunke. Mikroelektródy umožňujú zaznamenávať elektrické procesy v jednom jedinom neuróne alebo nervovom vlákne. Zvyčajne ide o sklenené kapiláry s veľmi tenkým hrotom s priemerom menším ako 1 µm, naplnené elektricky vodivým roztokom (napríklad chloridom draselným).
Ak sú na povrchu článku umiestnené dve elektródy, nezaznamená sa medzi nimi žiadny potenciálny rozdiel. Ak ale jedna z elektród prerazí cytoplazmatickú membránu neurónu (t.j. hrot elektródy je vo vnútornom prostredí), voltmeter zaznamená potenciálny skok až do približne -70 mV (obr. 7). Tento potenciál sa nazýva membránový potenciál. Môže byť zaregistrovaný nielen v neurónoch, ale v menej výraznej forme aj v iných bunkách tela. Ale iba v nervových, svalových a žľazových bunkách sa membránový potenciál môže zmeniť v reakcii na pôsobenie dráždidla. V tomto prípade sa nazýva membránový potenciál bunky, ktorý nie je ovplyvnený žiadnym stimulom oddychový potenciál(PP). V rôznych nervových bunkách je hodnota PP odlišná. Pohybuje sa od -50 do -100 mV. Čo spôsobuje tento PP?
Počiatočný (pred rozvojom PP) stav neurónu možno charakterizovať ako bez vnútorného náboja, t.j. počet katiónov a aniónov v cytoplazme bunky je rovnaký v dôsledku prítomnosti veľkých organických aniónov, pre ktoré je membrána neurónu nepriepustná. V skutočnosti sa takýto obraz pozoruje v počiatočných štádiách embryonálneho vývoja nervového tkaniva. Potom, keď dozrieva, sú zapnuté gény, ktoré spúšťajú syntézu. trvalo otvorené K+ kanály. Ióny K+ po ich zabudovaní do membrány dostávajú vďaka difúzii možnosť voľne opustiť bunku (kde ich je veľa) do medzibunkového prostredia (kde ich je oveľa menej).
Ale to nevedie k rovnováhe koncentrácií draslíka vo vnútri a mimo bunky, pretože. uvoľnenie katiónov vedie k tomu, že v bunke zostáva stále viac nekompenzovaných negatívnych nábojov. To spôsobuje vznik elektrického potenciálu, ktorý zabraňuje uvoľňovaniu nových kladne nabitých iónov. Výsledkom je, že uvoľňovanie draslíka pokračuje, kým sa sila koncentračného tlaku draslíka, vďaka ktorému opúšťa bunku, a pôsobenie elektrického poľa, ktoré tomu bráni, nevyrovnajú. V dôsledku toho vzniká potenciálny rozdiel medzi vonkajším a vnútorným prostredím bunky alebo rovnovážny draslíkový potenciál, ktorý je popísaný Nernstova rovnica:
EK = (RT / F) (ln [K+]o / [K+ ]i),
kde R je plynová konštanta, T je absolútna teplota, F je Faradayovo číslo, [K+]o je koncentrácia draselných iónov vo vonkajšom roztoku, [K+ ]i je koncentrácia draselných iónov v bunke.
Rovnica potvrdzuje závislosť, ktorá sa dá odvodiť aj logickým uvažovaním – čím väčší je rozdiel v koncentráciách draselných iónov vo vonkajšom a vnútornom prostredí, tým je väčší (v absolútnej hodnote) PP.
Klasické štúdie PP sa uskutočnili na obrovských axónoch chobotnice. Ich priemer je asi 0,5 mm, takže celý obsah axónu (axoplazmy) možno bez problémov odstrániť a axón naplniť roztokom draslíka, ktorého koncentrácia zodpovedá jeho vnútrobunkovej koncentrácii. Samotný axón bol umiestnený do roztoku draslíka s koncentráciou zodpovedajúcou medzibunkovému médiu. Potom sa zaznamenal RI, ktorý sa ukázal ako -75 mV. Rovnovážny draslíkový potenciál vypočítaný Nernstovou rovnicou pre tento prípad sa ukázal byť veľmi blízky tomu, ktorý bol získaný v experimente.
Ale RI v axóne chobotnice naplnenej skutočnou axoplazmou je približne -60 mV . Odkiaľ pochádza rozdiel 15 mV? Ukázalo sa, že na tvorbe PP sa podieľajú nielen draselné, ale aj sodné ióny. Faktom je, že okrem draslíkových kanálov obsahujú aj neurónové membrány trvalo otvorené sodíkové kanály. Je ich oveľa menej ako draslíkových, membrána však stále umožňuje vstup do bunky malému množstvu iónov Na +, a preto je vo väčšine neurónov RP -60-(-65) mV. Prúd sodíka je tiež úmerný rozdielu medzi jeho koncentráciami vo vnútri a mimo bunky – teda čím menší je tento rozdiel, tým väčšia je absolútna hodnota PP. Sodíkový prúd závisí aj od samotného PP. Okrem toho cez membránu difunduje veľmi malé množstvo Cl- iónov. Preto pri výpočte skutočného PP je Nernstova rovnica doplnená o údaje o koncentráciách iónov sodíka a chlóru vo vnútri a mimo článku. V tomto prípade sa vypočítané ukazovatele ukazujú ako veľmi blízke experimentálnym, čo potvrdzuje správnosť vysvetlenia pôvodu PP difúziou iónov cez neurónovú membránu.
Konečná úroveň pokojového potenciálu je teda určená spolupôsobením veľkého množstva faktorov, z ktorých hlavnými sú prúdy K +, Na + a aktivita sodno-draselnej pumpy. Výsledná hodnota PP je výsledkom dynamickej rovnováhy týchto procesov. Pôsobením na ktorýkoľvek z nich je možné posunúť úroveň PP a tým aj úroveň excitability nervovej bunky.
V dôsledku vyššie popísaných dejov je membrána neustále v stave polarizácie - jej vnútorná strana je nabitá záporne vzhľadom na vonkajšiu. Proces znižovania rozdielu potenciálov (t. j. znižovanie PP v absolútnej hodnote) sa nazýva depolarizácia a jeho zvýšenie (zvýšenie PP v absolútnej hodnote) sa nazýva hyperpolarizácia.
Dátum zverejnenia: 09.10.2015; Prečítané: 361 | Porušenie autorských práv stránky
studopedia.org – Studopedia.Org – 2014 – 2018. (0,002 s) ...
2–1. Pokojový membránový potenciál je:
1) potenciálny rozdiel medzi vonkajším a vnútorným povrchom bunkovej membrány v stave funkčného pokoja *
2) charakteristický znak iba buniek excitabilných tkanív
3) rýchle kolísanie náboja bunkovej membrány s amplitúdou 90-120 mV
4) potenciálny rozdiel medzi excitovanými a neexcitovanými úsekmi membrány
5) potenciálny rozdiel medzi poškodenými a nepoškodenými časťami membrány
2–2. V stave fyziologického pokoja je vnútorný povrch membrány excitabilnej bunky vo vzťahu k vonkajšiemu nabitý:
1) pozitívne
2), ako aj vonkajší povrch membrány
3) negatívne*
4) je bez poplatku
5) neexistuje správna odpoveď
2–3. Pozitívny posun (pokles) pokojového membránového potenciálu pôsobením stimulu sa nazýva:
1) hyperpolarizácia
2) repolarizácia
3) povznesenie
4) depolarizácia*
5) statická polarizácia
2–4. Negatívny posun (zvýšenie) pokojového membránového potenciálu sa nazýva:
1) depolarizácia
2) repolarizácia
3) hyperpolarizácia*
4) povznesenie
5) reverzia
2–5. Zostupná fáza akčného potenciálu (repolarizácia) je spojená so zvýšením priepustnosti membrány pre ióny:
2) vápnik
2–6. Vo vnútri bunky v porovnaní s medzibunkovou tekutinou je koncentrácia iónov vyššia:
3) vápnik
2–7. Zvýšenie prúdu draslíka počas vývoja akčného potenciálu spôsobuje:
1) rýchla repolarizácia membrány*
2) depolarizácia membrány
3) obrátenie membránového potenciálu
4) stopová depolarizácia
5) lokálna depolarizácia
2–8. Pri úplnej blokáde rýchlych sodíkových kanálov bunkovej membrány sa pozoruje nasledovné:
1) znížená excitabilita
2) zníženie amplitúdy akčného potenciálu
3) absolútna žiaruvzdornosť*
4) povznesenie
5) stopová depolarizácia
2–9. Záporný náboj na vnútornej strane bunkovej membrány vzniká v dôsledku difúzie:
1) K+ z bunky a elektrogénna funkcia K-Na pumpy *
2) Na+ do klietky
3) C1 - z bunky
4) Ca2+ do bunky
5) neexistuje správna odpoveď
2–10. Hodnota pokojového potenciálu je blízka hodnote rovnovážneho potenciálu pre ión:
3) vápnik
2–11. Rastúca fáza akčného potenciálu je spojená so zvýšením priepustnosti iónov:
2) neexistuje správna odpoveď
3) sodík*
2–12. Uveďte funkčnú úlohu pokojového membránového potenciálu:
1) jeho elektrické pole ovplyvňuje stav proteínových kanálov a membránových enzýmov*
2) charakterizuje zvýšenie excitability buniek
3) je hlavnou jednotkou kódovania informácií v nervovom systéme
4) zabezpečuje prevádzku membránových čerpadiel
5) charakterizuje zníženie excitability buniek
2–13. Schopnosť buniek reagovať na pôsobenie podnetov špecifickou reakciou, charakterizovanou rýchlou, reverzibilnou depolarizáciou membrány a zmenou metabolizmu, sa nazýva:
1) podráždenosť
2) vzrušivosť*
3) labilita
4) vodivosť
5) automatizácia
2–14. Biologické membrány, ktoré sa podieľajú na zmene intracelulárneho obsahu a intracelulárnych reakciách v dôsledku príjmu extracelulárnych biologicky aktívnych látok, vykonávajú funkciu:
1) bariéra
2) receptor-regulačný *
3) doprava
4) diferenciácia buniek
2–15. Minimálna sila stimulu potrebná a dostatočná na to, aby došlo k reakcii, sa nazýva:
1) prah*
2) superprah
3) submaximálne
4) podprahové
5) maximálne
2–16. So zvýšením prahu podráždenia, excitabilita bunky:
1) zvýšená
2) znížené*
3) sa nezmenil
4) všetko je správne
5) neexistuje správna odpoveď
2–17. Biologické membrány, podieľajúce sa na premene vonkajších podnetov neelektrickej a elektrickej povahy na bioelektrické signály, plnia najmä funkciu:
1) bariéra
2) regulačné
3) diferenciácia buniek
4) doprava
5) generovanie akčného potenciálu*
2–18. Akčný potenciál je:
1) stabilný potenciál, ktorý vzniká na membráne, keď sú dve sily v rovnováhe: difúzna a elektrostatická
2) potenciál medzi vonkajším a vnútorným povrchom bunky v stave funkčného pokoja
3) rýchle, aktívne sa šíriace, fázové kolísanie membránového potenciálu, sprevádzané spravidla dobíjaním membrány *
4) mierna zmena membránového potenciálu pôsobením podprahového stimulu
5) predĺžená, kongestívna depolarizácia membrány
2–19. Priepustnosť membrány pre Na+ vo fáze depolarizácie akčného potenciálu:
1) prudko stúpa a do bunky vstupuje silný sodíkový prúd *
2) prudko klesá a objavuje sa silný sodíkový prúd opúšťajúci bunku
3) sa výrazne nemení
4) všetko je správne
5) neexistuje správna odpoveď
2–20. Biologické membrány, ktoré sa podieľajú na uvoľňovaní neurotransmiterov v synaptických zakončeniach, vykonávajú najmä funkciu:
1) bariéra
2) regulačné
3) medzibunková interakcia*
4) receptor
5) generovanie akčného potenciálu
2–21. Molekulárny mechanizmus, ktorý zabezpečuje odstránenie sodných iónov z cytoplazmy a zavedenie draselných iónov do cytoplazmy, sa nazýva:
1) napäťovo riadený sodíkový kanál
2) nešpecifický sodíkovo-draslíkový kanál
3) chemodependentný sodíkový kanál
4) sodíkovo-draslíková pumpa*
5) únikový kanál
2–22. Systém pohybu iónov cez membránu pozdĺž koncentračného gradientu, nie vyžadujúci priamy výdaj energie sa nazýva:
1) pinocytóza
2) pasívny transport*
3) aktívny transport
4) persorpcia
5) exocytóza
2–23. Úroveň membránového potenciálu, pri ktorej vzniká akčný potenciál, sa nazýva:
1) pokojový membránový potenciál
2) kritická úroveň depolarizácie*
3) stopová hyperpolarizácia
4) nulová úroveň
5) stopová depolarizácia
2–24. So zvýšením koncentrácie K + v extracelulárnom prostredí s pokojovým membránovým potenciálom v excitabilnej bunke dôjde k:
1) depolarizácia*
2) hyperpolarizácia
3) transmembránový potenciálny rozdiel sa nezmení
4) stabilizácia transmembránového potenciálneho rozdielu
5) neexistuje správna odpoveď
2–25. Najvýznamnejšia zmena pri vystavení rýchlemu blokátoru sodíkových kanálov bude:
1) depolarizácia (zníženie pokojového potenciálu)
2) hyperpolarizácia (zvýšený pokojový potenciál)
3) zníženie strmosti depolarizačnej fázy akčného potenciálu *
4) spomalenie fázy repolarizácie akčného potenciálu
5) neexistuje správna odpoveď
3. HLAVNÉ VZORKY DRÁŽDENIA
VZRUŠITEĽNÉ TKANIVÁ
3–1. Zákon, podľa ktorého so zvyšujúcou sa silou stimulu sa odozva postupne zvyšuje, až kým nedosiahne maximum, sa nazýva:
1) "všetko alebo nič"
2) pevnosť-trvanie
3) ubytovanie
4) sily (mocenské vzťahy) *
5) polárny
3–2. Zákon, podľa ktorého excitabilná štruktúra reaguje na prahové a nadprahové podnety maximálnou možnou odozvou, sa nazýva:
2) "všetko alebo nič" *
3) pevnosť-trvanie
4) ubytovanie
5) polárny
3–3. Minimálny čas, počas ktorého prúd rovnajúci sa dvojnásobku reobázy (dvojnásobok prahovej sily) spôsobí budenie, sa nazýva:
1) dobrý čas
2) ubytovanie
3) prispôsobenie
4) chronaxia*
5) labilita
3–4. Konštrukcia sa riadi zákonom sily:
1) srdcový sval
2) jediné nervové vlákno
3) jediné svalové vlákno
4) celý kostrový sval*
5) jedna nervová bunka
Zákon „Všetko alebo nič“ sa riadi štruktúrou:
1) celý kostrový sval
2) nervový kmeň
3) srdcový sval*
4) hladké svalstvo
5) nervové centrum
3–6. Adaptácia tkaniva na pomaly rastúci stimul sa nazýva:
1) labilita
2) funkčná mobilita
3) hyperpolarizácia
4) ubytovanie*
5) brzdenie
3–7. Parabiózna fáza parabiózy je charakterizovaná:
1) zníženie odozvy so zvýšením sily stimulu *
2) zníženie odozvy so znížením sily stimulu
3) zvýšenie odozvy so zvýšením sily stimulu
4) rovnaká odozva so zvýšením sily stimulu
5) nedostatok reakcie na podnety akejkoľvek sily
3–8. Prah podráždenia je indikátorom:
1) vzrušivosť*
2) kontraktilita
3) labilita
4) vodivosť
5) automatizácia
Dátum zverejnenia: 08.04.2015; Prečítané: 2728 | Porušenie autorských práv stránky
studopedia.org – Studopedia.Org – 2014 – 2018. (0,009 s) ...
ÚLOHA AKTÍVNEHO TRANSPORTU IÓNOV PRI TVORENÍ MEMBRÁNOVÉHO POTENCIÁLU
Jednou z výhod „ideálnej“ membrány, ktorá umožňuje prechod akéhokoľvek jedného iónu, je zachovanie membránového potenciálu po ľubovoľne dlhý čas bez výdaja energie, za predpokladu, že prenikajúci ión je spočiatku rozmiestnený nerovnomerne na oboch stranách membrány. Zároveň je membrána živých buniek v tej či onej miere priepustná pre všetky anorganické ióny prítomné v roztoku obklopujúcom bunku. Preto musia bunky
nejako udržiavame intracelulárnu koncentráciu iónov na určitej úrovni. Dostatočne výpovedné sú v tomto smere ióny sodíka, na príklade ktorých priepustnosti bola v predchádzajúcej časti analyzovaná odchýlka potenciálu svalovej membrány od rovnovážneho draslíkového potenciálu. Podľa nameraných koncentrácií sodíkových iónov mimo a vo vnútri svalovej bunky bude rovnovážny potenciál vypočítaný Nernstovou rovnicou pre tieto ióny asi 60 mV a so znamienkom plus vo vnútri bunky. Membránový potenciál, vypočítaný podľa Goldmanovej rovnice a meraný pomocou mikroelektród, je 90 mV so znamienkom mínus vo vnútri článku. Jeho odchýlka od rovnovážneho potenciálu pre ióny sodíka bude teda 150 mV. Pri pôsobení takého vysokého potenciálu, dokonca aj pri nízkej permeabilite, sodíkové ióny vstúpia cez membránu a hromadia sa vo vnútri bunky, čo bude sprevádzané uvoľňovaním iónov draslíka z nej. V dôsledku tohto procesu sa intra- a extracelulárne koncentrácie iónov po určitom čase vyrovnajú.
V živej bunke sa to v skutočnosti nedeje, keďže sodíkové ióny sa z bunky neustále odstraňujú pomocou takzvanej iónovej pumpy. Predpoklad o existencii iónovej pumpy predložil R. Dean v 40-tych rokoch XX storočia. a bol mimoriadne dôležitým doplnkom k membránovej teórii tvorby pokojového potenciálu v živých bunkách. Experimentálne sa ukázalo, že aktívne „odčerpávanie“ Na + z bunky prichádza s povinným „odčerpávaním“ draselných iónov do bunky (obr. 2.8). Keďže priepustnosť membrány pre sodíkové ióny je malá, ich vstup z vonkajšieho prostredia do bunky bude prebiehať pomaly, preto
![]() Nízka koncentrácia K+ Vysoká koncentrácia Na++
Nízka koncentrácia K+ Vysoká koncentrácia Na++
pumpa bude účinne udržiavať nízku koncentráciu sodíkových iónov v bunke. Priepustnosť membrány pre draselné ióny v pokoji je pomerne vysoká a ľahko difundujú cez membránu.
Na udržanie vysokej koncentrácie draselných iónov nie je potrebné míňať energiu, tá sa udržiava vďaka vznikajúcemu transmembránovému rozdielu potenciálu, ktorého mechanizmy sú podrobne opísané v predchádzajúcich častiach. Prenos iónov pumpou vyžaduje vynaloženie metabolickej energie bunky. Zdrojom energie tohto procesu je energia uložená v makroergických väzbách molekúl ATP. Energia sa uvoľňuje hydrolýzou ATP pomocou enzýmu adenozíntrifosfatáza. Predpokladá sa, že ten istý enzým priamo vykonáva prenos iónov. V súlade so štruktúrou bunkovej membrány je ATPáza jedným z integrálnych proteínov zabudovaných do lipidovej dvojvrstvy. Charakteristickým znakom nosného enzýmu je jeho vysoká afinita na vonkajšom povrchu k draselným iónom a na vnútornom povrchu k sodným iónom. Pôsobenie inhibítorov oxidačných procesov (kyanidov alebo azidov) na bunku, ochladzovanie bunky blokuje hydrolýzu ATP, ako aj aktívny prenos sodných a draselných iónov. Do bunky postupne vstupujú sodné ióny a draselné ióny z nej odchádzajú a so znižovaním pomeru [K +] o / [K +], - bude pokojový potenciál pomaly klesať k nule. Diskutovali sme o situácii, keď iónová pumpa odstraňuje jeden kladne nabitý sodíkový ión z vnútrobunkového prostredia a podľa toho prenáša jeden kladne nabitý draselný ión z extracelulárneho priestoru (pomer 1: 1). V tomto prípade sa hovorí o iónovej pumpe elektricky neutrálny.
Zároveň sa experimentálne zistilo, že v niektorých nervových bunkách odoberie iónová pumpa za rovnaký čas viac iónov sodíka, ako pumpuje ióny draslíka (pomer môže byť 3:2). V takýchto prípadoch je iónová pumpa elektrogénny, t.
Physiologia_Answer
To znamená, že on sám vytvára malý, ale konštantný celkový prúd kladných nábojov z bunky a navyše v nej prispieva k vytvoreniu negatívneho potenciálu. Všimnite si, že dodatočný potenciál vytvorený elektrogénnou pumpou v pokojovej bunke nepresahuje niekoľko milivoltov.
Zhrňme si informácie o mechanizmoch vzniku membránového potenciálu – pokojového potenciálu v bunke. Hlavným procesom, vďaka ktorému sa väčšina potenciálu so záporným znamienkom vytvára na vnútornom povrchu bunkovej membrány, je výskyt elektrického potenciálu, ktorý oneskoruje pasívny výstup iónov draslíka z bunky pozdĺž jej koncentračného gradientu cez draslík. kanály - v -
 |
tegrálne proteíny. Iné ióny (napríklad sodné ióny) sa podieľajú na vytváraní potenciálu len v malej miere, pretože priepustnosť membrány je pre ne oveľa nižšia ako pre ióny draslíka, t.j. počet otvorených kanálov pre tieto ióny v pokoji je malý. Mimoriadne dôležitou podmienkou pre udržanie pokojového potenciálu je prítomnosť v bunke (v bunkovej membráne) iónovej pumpy (integrálneho proteínu), ktorá zabezpečuje koncentráciu sodíkových iónov vo vnútri bunky na nízkej úrovni a tým vytvára predpoklady pre hlavnými intracelulárnymi iónmi tvoriacimi potenciál sa stávajú ióny draslíka. Malý príspevok k pokojovému potenciálu môže urobiť priamo samotná iónová pumpa, ale pod podmienkou, že jej práca v bunke je elektrogénna.
Koncentrácia iónov vo vnútri a mimo bunky
Existujú teda dve skutočnosti, ktoré je potrebné vziať do úvahy, aby sme pochopili mechanizmy, ktoré udržiavajú pokojový membránový potenciál.
1 . Koncentrácia draselných iónov v bunke je oveľa vyššia ako v extracelulárnom prostredí. 2 . Membrána v pokoji je selektívne priepustná pre K+ a pre Na+ je priepustnosť membrány v pokoji zanedbateľná. Ak vezmeme priepustnosť draslíka ako 1, potom priepustnosť sodíka v pokoji bude len 0,04. teda dochádza k konštantnému toku iónov K+ z cytoplazmy pozdĺž koncentračného gradientu. Draslíkový prúd z cytoplazmy vytvára relatívny deficit kladných nábojov na vnútornom povrchu, pre anióny je bunková membrána nepriepustná, následkom čoho sa cytoplazma bunky nabije negatívne vzhľadom na prostredie obklopujúce bunku. Tento potenciálny rozdiel medzi bunkou a extracelulárnym priestorom, polarizácia bunky, sa nazýva pokojový membránový potenciál (RMP).
Vynára sa otázka: prečo prúd iónov draslíka nepokračuje, kým sa koncentrácie iónov mimo a vnútri bunky nevyrovnajú? Malo by sa pamätať na to, že ide o nabitú časticu, preto jej pohyb závisí aj od náboja membrány. Vnútrobunkový negatívny náboj, ktorý vzniká prúdom iónov draslíka z bunky, bráni novým iónom draslíka opustiť bunku. Tok draselných iónov sa zastaví, keď pôsobenie elektrického poľa kompenzuje pohyb iónu pozdĺž koncentračného gradientu. Preto pri danom rozdiele koncentrácií iónov na membráne vzniká pre draslík takzvaný ROVNOVÁHA POTENCIÁL. Tento potenciál (Ek) sa rovná RT/nF *ln /, (n je valencia iónu.) alebo
Ek=61,5 log/
Membránový potenciál (MP) do značnej miery závisí od rovnovážneho potenciálu draslíka, avšak časť sodíkových iónov stále preniká do pokojovej bunky, ako aj chloridové ióny. Záporný náboj, ktorý má bunková membrána, teda závisí od rovnovážnych potenciálov sodíka, draslíka a chlóru a je opísaný Nernstovou rovnicou. Prítomnosť tohto pokojového membránového potenciálu je mimoriadne dôležitá, pretože určuje schopnosť bunky excitovať – špecifickú odpoveď na podnet.
bunková excitácia
AT vzrušenie buniek (prechod z pokoja do aktívneho stavu) nastáva so zvýšením permeability iónových kanálov pre sodík a niekedy aj pre vápnik. Dôvodom zmeny permeability môže byť zmena potenciálu membrány - aktivujú sa elektricky excitovateľné kanály a interakcia membránových receptorov s biologicky aktívnou látkou - receptormi - riadené kanály a mechanické pôsobenie. V každom prípade pre rozvoj vzrušenia je to nevyhnutné počiatočná depolarizácia - mierny pokles záporného náboja membrány, spôsobené pôsobením podnetu. Dráždivou látkou môže byť akákoľvek zmena parametrov vonkajšieho alebo vnútorného prostredia tela: svetlo, teplota, chemikálie (vplyv na chuťové a čuchové receptory), naťahovanie, tlak. Sodík prúdi do bunky, dochádza k iónovému prúdu a membránový potenciál klesá - depolarizácia membrány.
Tabuľka 4
Zmena membránového potenciálu počas bunkovej excitácie.
Venujte pozornosť skutočnosti, že sodík vstupuje do bunky pozdĺž koncentračného gradientu a pozdĺž elektrického gradientu: koncentrácia sodíka v bunke je 10-krát nižšia ako v extracelulárnom prostredí a náboj vo vzťahu k extracelulárnemu je negatívny. Súčasne sú aktivované aj draslíkové kanály, ale sodíkové (rýchle) sú aktivované a inaktivované v priebehu 1–1,5 milisekúnd a draslíkové kanály trvajú dlhšie.
Zmeny membránového potenciálu sú zvyčajne znázornené graficky. Horný obrázok znázorňuje počiatočnú depolarizáciu membrány – zmenu potenciálu v reakcii na pôsobenie stimulu. Pre každú excitabilnú bunku existuje špeciálna úroveň membránového potenciálu, po dosiahnutí ktorej sa vlastnosti sodíkových kanálov dramaticky menia. Tento potenciál je tzv kritická úroveň depolarizácie (KUD). Keď sa membránový potenciál zmení na KUD, otvoria sa rýchle, na potenciáli závislé sodíkové kanály, tok sodíkových iónov sa ponáhľa do bunky. S prechodom kladne nabitých iónov do bunky v cytoplazme sa kladný náboj zvyšuje. V dôsledku toho sa transmembránový potenciálny rozdiel znižuje, hodnota MP sa znižuje na 0 a potom, keď sodík ďalej vstupuje do bunky, membrána sa znovu nabije a náboj sa obráti (prestrelí) - teraz sa povrch stáva elektronegatívnym vzhľadom na cytoplazmu - membrána je úplne DEPOLARIZOVANÁ - stredná postava. Nedochádza k ďalšej zmene poplatkov, pretože sodíkové kanály sú inaktivované- viac sodíka nemôže vstúpiť do bunky, hoci koncentračný gradient sa mení veľmi mierne. Ak má stimul takú silu, že depolarizuje membránu na FCD, tento stimul sa nazýva prahový stimul, spôsobuje excitáciu bunky. Potenciálny bod zvratu je znakom toho, že celý rozsah podnetov akejkoľvek modality bol preložený do jazyka nervového systému – excitačné impulzy. Impulzy alebo excitačné potenciály sa nazývajú akčné potenciály. Akčný potenciál (AP) – rýchla zmena membránového potenciálu v reakcii na pôsobenie prahového stimulu. AP má štandardné parametre amplitúdy a času, ktoré nezávisia od sily stimulu – pravidlo „ALL OR NIČ“. Ďalšou fázou je obnovenie pokojového membránového potenciálu - repolarizácia(dolný obrázok) je spôsobený hlavne aktívnym transportom iónov. Najdôležitejším procesom aktívneho transportu je práca Na/K – pumpy, ktorá pumpuje sodíkové ióny von z bunky a súčasne pumpuje do bunky draselné ióny. Obnovenie membránového potenciálu nastáva v dôsledku prúdu draslíkových iónov z bunky - aktivujú sa draslíkové kanály a umožňujú draslíkovým iónom prechádzať, kým sa nedosiahne rovnovážny draslíkový potenciál. Tento proces je dôležitý, pretože kým sa MPP neobnoví, bunka nie je schopná vnímať nový excitačný impulz.
HYPERPOLARIZÁCIA - krátkodobé zvýšenie MP po jej obnovení, čo je spôsobené zvýšením priepustnosti membrány pre ióny draslíka a chlóru. Hyperpolarizácia nastáva až po PD a nie je charakteristická pre všetky bunky. Skúsme ešte raz graficky znázorniť fázy akčného potenciálu a iónové procesy, ktoré sú základom zmien membránového potenciálu (obr.
Pokojový potenciál neurónu
deväť). Na osi x vynesme hodnoty membránového potenciálu v milivoltoch a na zvislú os čas v milisekundách.
1. Depolarizácia membrány na KUD - môžu sa otvoriť akékoľvek sodíkové kanály, niekedy vápnikové, rýchle aj pomalé, závislé od napätia a riadené receptormi. Závisí to od typu stimulu a typu bunky.
2. Rýchly vstup sodíka do bunky - rýchle, napäťovo závislé sodíkové kanály sa otvárajú a depolarizácia dosiahne bod obratu potenciálu - membrána sa znovu nabije, znamienko náboja sa zmení na kladné.
3. Obnova koncentračného gradientu draslíka - prevádzka čerpadla. Draslíkové kanály sú aktivované, draslík prechádza z bunky do extracelulárneho prostredia - začína sa repolarizácia, obnova MPP
4. Stopová depolarizácia alebo negatívny stopový potenciál – membrána je stále depolarizovaná vzhľadom na MPP.
5. Hyperpolarizácia stopy. Draslíkové kanály zostávajú otvorené a dodatočný draslíkový prúd hyperpolarizuje membránu. Potom sa bunka vráti na počiatočnú úroveň MPP. Trvanie AP je pre rôzne bunky od 1 do 3-4 ms.

Obrázok 9 Fázy akčného potenciálu
Všimnite si tri potenciálne hodnoty, ktoré sú dôležité a konštantné pre každú bunku jej elektrických charakteristík.
1. MPP - elektronegativita bunkovej membrány v pokoji, poskytujúca schopnosť excitácie - excitabilita. Na obrázku MPP \u003d -90 mV.
2. KUD - kritická úroveň depolarizácie (alebo prah pre generovanie membránového akčného potenciálu) - je to hodnota membránového potenciálu, pri ktorej sa otvoria rýchlo, potenciálne závislé sodíkové kanály a membrána sa znovu nabije v dôsledku vstupu kladných sodíkových iónov do bunky. Čím vyššia je elektronegativita membrány, tým je ťažšie ju depolarizovať na FCD, tým je takýto článok menej excitabilný.
3. Potenciálny bod zvratu (prekmit) - taká hodnota pozitívne membránový potenciál, pri ktorom kladne nabité ióny už neprenikajú do bunky – krátkodobý rovnovážny sodíkový potenciál. Na obrázku + 30 mV. Celková zmena membránového potenciálu z –90 na +30 bude pre danú bunku 120 mV, táto hodnota je akčný potenciál. Ak tento potenciál vznikol v neuróne, rozšíri sa pozdĺž nervového vlákna, ak sa vo svalových bunkách rozšíri po membráne svalového vlákna a povedie ku kontrakcii, v žľazovom k sekrécii – k pôsobeniu bunky. Toto je špecifická odpoveď bunky na pôsobenie stimulu, excitácia.
Pri vystavení podnetu podprahová pevnosť dochádza k neúplnej depolarizácii - LOCAL RESPONSE (LO).
Neúplná alebo čiastočná depolarizácia je zmena v náboji membrány, ktorá nedosahuje kritickú úroveň depolarizácie (CDL).

Obrázok 10. Zmena membránového potenciálu ako odpoveď na pôsobenie stimulu podprahovej sily – lokálna odpoveď
Lokálna odpoveď má v podstate rovnaký mechanizmus ako AP, jej vzostupná fáza je určená vstupom sodíkových iónov a zostupná fáza je určená výstupom draselných iónov.
Amplitúda LO je však úmerná sile podprahovej stimulácie a nie je štandardná, ako pri PD.
Tabuľka 5
Je ľahké vidieť, že v bunkách existujú podmienky, za ktorých by mal vzniknúť potenciálny rozdiel medzi bunkou a medzibunkovým médiom:
1) bunkové membrány sú dobre priepustné pre katióny (predovšetkým draslík), zatiaľ čo priepustnosť membrán pre anióny je oveľa menšia;
2) koncentrácie väčšiny látok v bunkách a v medzibunkovej tekutine sú veľmi odlišné (porovnaj s tým, čo bolo povedané na str.
). Preto sa na bunkových membránach objaví dvojitá elektrická vrstva („mínus“ na vnútornej strane membrány, „plus“ na vonkajšej strane) a na membráne musí existovať konštantný potenciálny rozdiel, ktorý sa nazýva pokojový potenciál. Membrána je vraj v pokoji polarizovaná.
Prvýkrát bola hypotéza o podobnej povahe PP buniek a difúznom potenciáli Nernsta vyjadrená v roku 1896.
Vedomostná základňa
študent Vojenskej lekárskej akadémie Yu.V. Chagovets. Teraz je tento názor potvrdený mnohými experimentálnymi údajmi. Je pravda, že medzi nameranými hodnotami PP a hodnotami vypočítanými pomocou vzorca (1) existujú určité nezrovnalosti, ale sú vysvetlené dvoma zrejmými dôvodmi. Po prvé, v bunkách nie je jeden katión, ale veľa (K, Na, Ca, Mg atď.). Dá sa to vziať do úvahy nahradením Nernstovho vzorca (1) komplexnejším vzorcom, ktorý zhltol Goldman:
Kde pK je priepustnosť membrány pre draslík, pNa je rovnaké pre sodík, pCl je rovnaké pre chlór; [K + ] e je koncentrácia draselných iónov mimo článku, [K + ] i je rovnaká vo vnútri článku (podobne ako sodík a chlór); elipsa označuje zodpovedajúce výrazy pre iné ióny. Ióny chlóru (a iné anióny) idú opačným smerom ako ióny draslíka a sodíka, takže znamienka „e“ a „i“ sú pre ne v opačnom poradí.
Výpočet pomocou Goldmanovho vzorca poskytuje oveľa lepšiu zhodu s experimentom, ale stále pretrvávajú niektoré nezrovnalosti. Vysvetľuje to skutočnosť, že pri odvodzovaní vzorca (2) sa nezohľadnila práca aktívneho transportu. Účtovanie týchto údajov umožňuje dosiahnuť takmer úplnú zhodu s experimentom.
19. Sodíkové a draslíkové kanály v membráne a ich úloha v bioelektrogenéze. Mechanizmus brány. Vlastnosti potenciálne závislých kanálov. Mechanizmus akčného potenciálu. Stav kanálov a povaha tokov iónov v rôznych fázach PD. Úloha aktívneho transportu v bioelektrogenéze. Kritický membránový potenciál. Zákon všetko alebo nič pre vzrušivé membrány. Žiaruvzdorné.
Ukázalo sa, že selektívny filter má „tuhú“ štruktúru, to znamená, že za rôznych podmienok nemení svoju vôľu. Prechody kanála z otvoreného na zatvorený a naopak súvisia s činnosťou neselektívneho filtra, hradlového mechanizmu. Pod hradlovými procesmi vyskytujúcimi sa v jednej alebo druhej časti iónového kanála, ktorý sa nazýva brána, rozumieme akékoľvek zmeny v konformácii proteínových molekúl, ktoré tvoria kanál, v dôsledku čoho sa jeho pár môže otvárať alebo zatvárať. Preto je zvykom nazývať bránu funkčnými skupinami proteínových molekúl, ktoré zabezpečujú procesy brány. Dôležité je, aby brány uvádzali do pohybu fyziologické podnety, teda tie, ktoré sú prítomné v prirodzených podmienkach. Medzi fyziologickými stimulmi zohrávajú zvláštnu úlohu posuny membránového potenciálu.
Existujú kanály, ktoré sú riadené potenciálnym rozdielom na membráne, pričom sú pri niektorých hodnotách membránového potenciálu otvorené a pri iných zatvorené. Takéto kanály sa nazývajú potenciálne závislé. Práve s nimi je spojené generovanie PD. Všetky iónové kanály biomembrán sú vďaka svojmu osobitnému významu rozdelené do 2 typov: napäťovo závislé a napäťovo nezávislé. Prirodzenými stimulmi, ktoré riadia pohyb brány v kanáloch druhého typu, nie sú posuny membránového potenciálu, ale iné faktory. Napríklad v chemosenzitívnych kanáloch patrí úloha kontrolného stimulu chemikáliám.
Základnou súčasťou napäťovo riadeného iónového kanála je snímač napätia. Toto je názov skupiny proteínových molekúl, ktoré môžu reagovať na zmeny v elektrickom poli. Zatiaľ neexistujú žiadne konkrétne informácie o tom, čo sú a ako sa nachádzajú, ale je jasné, že elektrické pole môže vo fyzickom prostredí interagovať iba s nábojmi (či už voľnými alebo viazanými). Predpokladalo sa, že Ca2+ (voľné náboje) slúži ako napäťový senzor, keďže zmeny jeho obsahu v medzibunkovej tekutine vedú k rovnakým dôsledkom ako posuny membránového potenciálu. Napríklad desaťnásobný pokles koncentrácie vápenatých iónov v interstíciu je ekvivalentný depolarizácii plazmatickej membrány o približne 15 mV. Neskôr sa však ukázalo, že Ca2+ je potrebný na fungovanie snímača napätia, ale nie je sám osebe. PD sa vytvára aj vtedy, keď koncentrácia voľného vápnika v medzibunkovom médiu klesne pod 10~8 mol. Okrem toho obsah Ca2+ v cytoplazme má vo všeobecnosti malý vplyv na iónovú vodivosť plazmatickej membrány. Je zrejmé, že na napäťový senzor sú viazané náboje - skupiny proteínových molekúl s veľkým dipólovým momentom. Sú vložené do lipidovej dvojvrstvy, ktorá sa vyznačuje skôr nízkou viskozitou (30 - 100 cP) a nízkou dielektrickou konštantou. Tento záver vyplynul zo štúdie kinetických charakteristík pohybu napäťového snímača s posunmi membránového potenciálu. Tento pohyb je typickým posunovým prúdom.
Moderný funkčný model sodíkového napäťovo závislého kanála zabezpečuje existenciu dvoch typov brán, ktoré pracujú v protifáze. Líšia sa inerciálnymi vlastnosťami. Mobilnejšie (ľahké) sa nazývajú m-brány, viac zotrvačné (ťažké) - h - brány. V pokoji sú h-brány otvorené, m-brány zatvorené, pohyb Na+ kanálom je nemožný. Keď je plazmolema depolarizovaná, brány oboch typov sa začnú pohybovať, ale v dôsledku nerovnakej zotrvačnosti majú m-brány čas
otvorte pred zatvorením h-brány. V tomto momente je sodíkový kanál otvorený a Na + ním prúdi do bunky. Oneskorenie pohybu h-brány voči m-bráne zodpovedá trvaniu depolarizačnej fázy AP. Keď sa h-brána zatvorí, prietok Na + cez membránu sa zastaví a začne sa repolarizácia. Potom sa h - a m - brány vrátia do pôvodného stavu. Potenciálne závislé sodíkové kanály sa aktivujú (zapnú) počas rýchlej (skokovej) depolarizácie plazmatickej membrány. ,
PD vzniká vďaka rýchlejšej difúzii sodných iónov cez plazmatickú membránu v porovnaní s aniónmi, ktoré s ním tvoria soli v medzibunkovom prostredí. Preto je depolarizácia spojená so vstupom sodíkových katiónov do cytoplazmy. S rozvojom PD sa sodík v bunke nehromadí. Pri vzrušení dochádza k prichádzajúcemu a odchádzajúcemu toku sodíka. Výskyt AP nie je spôsobený porušením iónových koncentrácií v cytoplazme, ale poklesom elektrického odporu plazmatickej membrány v dôsledku zvýšenia jej permeability pre sodík.
Ako už bolo spomenuté, pôsobením prahových a nadprahových stimulov excitabilná membrána generuje AP. Tento proces je charakteristický zákona "všetko alebo nič. Je to protiklad postupnosti. Zmyslom zákona je, že parametre AP nezávisia od intenzity podnetu. Akonáhle sa dosiahne IMF, zmeny v potenciálnom rozdiele na excitovateľnej membráne sú určené iba vlastnosťami jej napäťovo riadených iónových kanálov, ktoré poskytujú prichádzajúci prúd. Medzi nimi vonkajší podnet otvára len tie najcitlivejšie. Iné sa otvárajú na úkor predchádzajúcich, už bez ohľadu na podnet. Hovoria o spantanovej povahe procesu zapájania stále nových potenciálne závislých iónových kanálov do transmembránového transportu iónov. Takže amplitúda. Trvanie a strmosť prednej a zadnej časti AP závisí iba od iónových gradientov na bunkovej membráne a kinetických charakteristík jej kanálov. Zákon všetko alebo nič je najcharakteristickejšou vlastnosťou jednotlivých buniek a vlákien, ktoré majú excitabilnú membránu. Nie je charakteristický pre väčšinu mnohobunkových útvarov. Výnimkou sú štruktúry organizované podľa typu syncýtia.
Dátum publikácie: 25.01.2015; Prečítané: 421 | Porušenie autorských práv stránky
studopedia.org – Studopedia.Org – 2014 – 2018. (0,001 s) ...
Článok do súťaže "bio/mol/text": Pokojový potenciál je dôležitým javom v živote všetkých telesných buniek a je dôležité vedieť, ako sa tvorí. Ide však o zložitý dynamický proces, ktorý je ako celok ťažko pochopiteľný najmä pre študentov bakalárskeho štúdia (biologické, lekárske a psychologické odbory) a nepripravených čitateľov. Pri zvažovaní bodov je však celkom možné pochopiť jeho hlavné detaily a fázy. Príspevok predstavuje koncept pokojového potenciálu a zdôrazňuje hlavné fázy jeho formovania pomocou obrazných metafor, ktoré pomáhajú pochopiť a zapamätať si molekulárne mechanizmy formovanie pokojového potenciálu.
Membránové transportné štruktúry – sodíkovo-draselné pumpy – vytvárajú predpoklady pre vznik pokojového potenciálu. Týmito predpokladmi je rozdiel v koncentrácii iónov na vnútornej a vonkajšej strane bunkovej membrány. Oddelene sa prejavuje rozdiel v koncentrácii sodíka a rozdiel v koncentrácii draslíka. Pokus iónov draslíka (K +) vyrovnať ich koncentráciu na oboch stranách membrány vedie k ich úniku z bunky a spolu s nimi aj strate kladných elektrických nábojov, čím vzniká celkový záporný náboj vnútorného povrchu membrány. bunka je výrazne zvýšená. Táto „draslíková“ negativita tvorí väčšinu pokojového potenciálu (-60 mV v priemere) a menšiu časť (-10 mV) tvorí „výmenná“ negativita spôsobená elektrogenitou samotnej iónomeničovej pumpy.
Poďme to pochopiť podrobnejšie.
Prečo potrebujeme vedieť, čo je to pokojový potenciál a ako vzniká?
Viete, čo je to „živočíšna elektrina“? Odkiaľ pochádzajú bioprúdy v tele? Ako sa môže živá bunka vo vodnom prostredí zmeniť na „elektrickú batériu“ a prečo sa okamžite nevybije?
Na tieto otázky možno odpovedať iba vtedy, ak zistíme, ako si bunka vytvára rozdiel v elektrických potenciáloch (kľudový potenciál) naprieč membránou.
Je celkom zrejmé, že na to, aby sme pochopili, ako funguje nervový systém, je najprv potrebné pochopiť, ako funguje jeho samostatná nervová bunka, neurón. Hlavná vec, ktorá je základom práce neurónu, je pohyb elektrických nábojov cez jeho membránu a v dôsledku toho výskyt elektrických potenciálov na membráne. Dá sa povedať, že neurón, ktorý sa pripravuje na svoju nervovú prácu, najskôr ukladá energiu v elektrickej forme a potom ju používa v procese vedenia a prenosu nervového vzruchu.
Naším prvým krokom pri štúdiu fungovania nervového systému je teda pochopenie toho, ako sa elektrický potenciál objavuje na membráne nervových buniek. To je to, čo urobíme, a nazveme tento proces tvorba pokojového potenciálu.
Definícia pojmu „potenciál odpočinku“
Normálne, keď je nervová bunka vo fyziologickom pokoji a pripravená pracovať, už prešla redistribúciou elektrických nábojov medzi vnútornou a vonkajšou stranou membrány. V dôsledku toho vzniklo elektrické pole a na membráne sa objavil elektrický potenciál - pokojový membránový potenciál.
Membrána je teda polarizovaná. To znamená, že má odlišný elektrický potenciál vonkajšieho a vnútorného povrchu. Je celkom možné zaregistrovať rozdiel medzi týmito potenciálmi.
Dá sa to overiť vložením mikroelektródy pripojenej k záznamovému zariadeniu do článku. Hneď ako elektróda vstúpi do článku, okamžite nadobudne určitý konštantný elektronegatívny potenciál vzhľadom na elektródu umiestnenú v tekutine obklopujúcej článok. Hodnota vnútrobunkového elektrického potenciálu v nervových bunkách a vláknach, napríklad nervových vláknach obrovských chobotníc, v pokoji je asi -70 mV. Táto hodnota sa nazýva pokojový membránový potenciál (RMP). Vo všetkých bodoch axoplazmy je tento potenciál prakticky rovnaký.
Nozdrachev A.D. atď. Začiatky fyziológie.
Trochu viac fyziky. makroskopické fyzické telá, sú spravidla elektricky neutrálne, t.j. obsahujú rovnaké množstvo kladných aj záporných nábojov. Teleso môžete nabiť tak, že v ňom vytvoríte prebytok nabitých častíc jedného typu, napríklad trením o iné teleso, pri ktorom sa v tomto prípade vytvorí prebytok nábojov opačného typu. Berúc do úvahy prítomnosť elementárneho náboja ( e), celkový elektrický náboj akéhokoľvek telesa možno znázorniť ako q= ±Nx e, kde N je celé číslo.
oddychový potenciál- to je rozdiel v elektrických potenciáloch dostupných na vnútornej a vonkajšej strane membrány, keď je bunka v stave fyziologického pokoja. Jeho hodnota sa meria zvnútra bunky, je záporná a má priemer -70 mV (milivoltov), hoci sa môže v rôznych bunkách líšiť: od -35 mV do -90 mV.
Je dôležité vziať do úvahy, že v nervovom systéme nie sú elektrické náboje reprezentované elektrónmi, ako v bežných kovových drôtoch, ale iónmi - chemickými časticami, ktoré majú elektrický náboj. A vo všeobecnosti v vodné roztoky Vo forme elektrického prúdu sa nepohybujú elektróny, ale ióny. Preto všetko elektrické prúdy v bunkách a ich prostredí je iónové prúdy.
Takže vo vnútri bunky v pokoji je záporne nabitá a vonku - kladne. To je charakteristické pre všetky živé bunky, snáď s výnimkou erytrocytov, ktoré sú naopak zvonku negatívne nabité. Presnejšie povedané, ukazuje sa, že pozitívne ióny (katióny Na + a K +) budú prevládať vonku okolo bunky a negatívne ióny (anióny organických kyselín, ktoré sa nemôžu voľne pohybovať cez membránu, ako Na + a K +) budú prevládať vo vnútri.
Teraz už len musíme vysvetliť, ako to všetko dopadlo. Aj keď je samozrejme nepríjemné uvedomiť si, že všetky naše bunky okrem erytrocytov vyzerajú len navonok pozitívne, no vo vnútri sú negatívne.
Pre jednoduchosť vysvetlenia zmien úrovne pokojového potenciálu sa nám bude hodiť pojem „negativita“, ktorým budeme charakterizovať elektrický potenciál vo vnútri bunky. Cenné v tomto termíne je, že nasledovné je intuitívne jasné: čím väčšia negativita vo vnútri bunky, tým nižšia in negatívna stránka potenciál je posunutý od nuly a čím je negatívum menšie, tým je negatívny potenciál bližšie k nule. Je to oveľa jednoduchšie pochopiť, ako zakaždým pochopiť, čo presne znamená výraz „potenciál sa zvyšuje“ - zvýšenie absolútnej hodnoty (alebo „modulo“) bude znamenať posun pokojového potenciálu smerom nadol od nuly, ale jednoducho „zvýšenie“ znamená posun potenciálu až na nulu. Pojem „negativita“ nevytvára podobné problémy s nejednoznačnosťou.
Podstata tvorby pokojového potenciálu
Skúsme prísť na to, odkiaľ pochádza elektrický náboj nervových buniek, hoci ich nikto nedrhne, ako to robia fyzici pri svojich experimentoch s elektrickými nábojmi.
Tu na výskumníka a študenta čaká jedna z logických pascí: vnútorná negativita bunky nevzniká z výskyt extra negatívnych častíc(anióny), ale naopak v dôsledku strata niektorých pozitívnych častíc(katióny)!
Kam teda odchádzajú kladne nabité častice z bunky? Pripomínam, že ide o ióny sodíka, ktoré opustili bunku a nahromadili sa vonku - Na + - a draselné ióny - K +.
Hlavné tajomstvo vzhľadu negativity vo vnútri bunky
Okamžite otvorme toto tajomstvo a povedzme, že bunka stráca časť svojich pozitívnych častíc a stáva sa záporne nabitá v dôsledku dvoch procesov:
- najprv vymení svoj „vlastný“ sodík za „cudzí“ draslík (áno, niektoré kladné ióny za iné, rovnako pozitívne);
- potom z nej unikajú tieto „pomenované“ kladné draselné ióny, spolu s ktorými z bunky unikajú kladné náboje.
Tieto dva procesy si musíme vysvetliť.
Prvá fáza vytvárania vnútornej negativity: výmena Na + za K +
Proteínové bielkoviny neustále pracujú v membráne nervovej bunky. výmenníkové čerpadlá(adenozíntrifosfatáza alebo Na+/K+-ATPáza), zapustené v membráne. Menia „vlastný“ sodík bunky na vonkajší „cudzí“ draslík.
No predsa pri výmene jedného kladného náboja (Na +) za iný s rovnakým kladným nábojom (K +) nemôže byť v článku núdza o kladné náboje! správne. Ale napriek tomu v dôsledku tejto výmeny zostáva v bunke veľmi málo iónov sodíka, pretože takmer všetky odišli von. A zároveň je bunka preplnená iónmi draslíka, ktoré do nej pumpovali molekulárne pumpy. Ak by sme mohli ochutnať cytoplazmu bunky, všimli by sme si, že v dôsledku práce výmenných púmp sa zmenila zo slanej na horko-slano-kyslú, pretože slanú chuť chloridu sodného nahradila komplexná chuť pomerne koncentrovaný roztok chloridu draselného. V bunke dosahuje koncentrácia draslíka 0,4 mol / l. Roztoky chloridu draselného v rozsahu 0,009-0,02 mol / l majú sladkú chuť, 0,03-0,04 - horkú, 0,05-0,1 - horko-slanú a od 0,2 a viac - komplexnú chuť, pozostávajúcu zo slanej, horkej a kyslé.
Dôležité je tu to výmena sodíka za draslík - nerov. Za každú danú bunku tri ióny sodíka dostane všetko dva draselné ióny. To má za následok stratu jedného kladného náboja pri každej iónovej výmene. Takže už v tomto štádiu bunka v dôsledku nerovnakej výmeny stráca viac „plusov“, ako dostáva na oplátku. V elektrickom vyjadrení to predstavuje približne -10 mV negativity vo vnútri bunky. (Pamätajte však, že stále musíme nájsť vysvetlenie pre zvyšných -60 mV!)
Na uľahčenie zapamätania si činnosti výmenníkových čerpadiel ju možno obrazne vyjadriť takto: "Bunka miluje draslík!" Preto bunka ťahá draslík k sebe, napriek tomu, že je ho už plná. A preto ho nerentabilne vymieňa za sodík, čím dáva 3 ióny sodíka za 2 ióny draslíka. A tak vynakladá na túto výmenu energiu ATP. A ako utrácať! Až 70 % všetkej spotreby energie neurónov možno minúť na prácu sodíkovo-draslíkových púmp. (To robí láska, aj keď to nie je skutočné!)
Mimochodom, je zaujímavé, že bunka sa nerodí s hotovým odpočinkovým potenciálom. Ešte ju potrebuje vytvoriť. Napríklad pri diferenciácii a fúzii myoblastov sa mení potenciál ich membrány z –10 na –70 mV, t.j. ich membrána sa stáva negatívnejšou – v procese diferenciácie sa polarizuje. A pri pokusoch na multipotentných mezenchymálnych stromálnych bunkách ľudskej kostnej drene umelá depolarizácia, ktorá pôsobí proti pokojovému potenciálu a znižuje negativitu buniek, dokonca inhibovala (deprimovala) diferenciáciu buniek.
Obrazne povedané, dá sa to vyjadriť takto: Vytvorením potenciálu na oddych sa bunka „nabije láskou“. Je to láska k dvom veciam:
- láska bunky k draslíku (preto ho bunka násilne ťahá k sebe);
- láska k draslíku k slobode (preto draslík opúšťa bunku, ktorá ho zachytila).
Mechanizmus saturácie buniek draslíkom sme si už vysvetlili (toto je práca výmenných púmp) a mechanizmus odchodu draslíka z bunky si vysvetlíme nižšie, keď pristúpime k popisu druhého štádia vytvárania vnútrobunkovej negativity. Takže výsledok činnosti membránových iónomeničových púmp v prvej fáze tvorby pokojového potenciálu je nasledovný:
- Nedostatok sodíka (Na +) v bunke.
- Nadbytok draslíka (K +) v bunke.
- Objavenie sa slabého elektrického potenciálu na membráne (–10 mV).
Môžeme povedať toto: v prvom štádiu iónové pumpy membrány vytvárajú rozdiel v koncentráciách iónov alebo koncentračný gradient (rozdiel) medzi intracelulárnym a extracelulárnym prostredím.
Druhá fáza vytvárania negativity: únik iónov K + z bunky
Čo teda začína v bunke potom, čo jej membránové čerpadlá sodíkovo-draslíkového výmenníka pracujú s iónmi?
Kvôli výslednému nedostatku sodíka vo vnútri bunky sa tento ión snaží pri každej príležitosti ponáhľať sa dovnútra: rozpustené látky majú vždy tendenciu vyrovnávať svoju koncentráciu v celom objeme roztoku. To však nefunguje dobre pre sodík, pretože sodíkové iónové kanály sú zvyčajne uzavreté a otvorené iba za určitých podmienok: pod vplyvom špeciálnych látok (vysielačov) alebo so znížením negativity v bunke (depolarizácia membrány).
Zároveň je v bunke nadbytok iónov draslíka v porovnaní s vonkajším prostredím – membránové pumpy ho totiž násilne pumpovali do bunky. A on, v snahe vyrovnať svoju koncentráciu zvnútra aj zvonka, sa naopak snaží, dostať von z cely. A darí sa mu to!
Draselné ióny K + opúšťajú bunku pôsobením chemického koncentračného gradientu na opačných stranách membrány (membrána je oveľa priepustnejšia pre K + ako pre Na +) a odnášajú so sebou kladné náboje. Kvôli tomu vo vnútri bunky rastie negativita.
Tu je tiež dôležité pochopiť, že ióny sodíka a draslíka sa navzájom „nevšimnú“, reagujú iba „na seba“. Tie. sodík reaguje na koncentráciu sodíka, ale "nedáva pozor" na to, koľko draslíka je v okolí. Naopak draslík reaguje len na koncentráciu draslíka a sodík si „nevšimne“. Ukazuje sa, že na pochopenie správania iónov je potrebné samostatne zvážiť koncentrácie sodíkových a draselných iónov. Tie. je potrebné zvlášť porovnávať koncentráciu sodíka vo vnútri a mimo bunky a zvlášť koncentráciu draslíka vo vnútri a mimo bunky, ale nemá zmysel porovnávať sodík s draslíkom, ako sa to deje v učebniciach.
Podľa zákona o vyrovnávaní chemických koncentrácií, ktorý funguje v roztokoch, sodík „chce“ vstúpiť do bunky zvonku; ťahá ho tam aj elektrická sila (ako si pamätáme, cytoplazma je negatívne nabitá). Chce niečo chcieť, ale nemôže, pretože membrána v normálnom stave neprechádza dobre. Kanály sodíkových iónov prítomné v membráne sú normálne uzavreté. Ak predsa len trochu vstúpi, bunka ho okamžite vymení za vonkajší draslík pomocou svojich sodíkovo-draslíkových výmenných púmp. Ukazuje sa, že ióny sodíka prechádzajú bunkou ako pri prechode a nezostávajú v nej. Preto je sodíka v neurónoch vždy nedostatok.
Ale draslík môže jednoducho odísť z bunky! Je ho plná klietka a ona si ho nemôže nechať. Vystupuje cez špeciálne kanály v membráne - "kanály úniku draslíka", ktoré sú normálne otvorené a uvoľňujú draslík.
Únikové kanály K+ sú neustále otvorené pri normálnych hodnotách pokojového membránového potenciálu a vykazujú výbuchy aktivity počas posunov membránového potenciálu, ktoré trvajú niekoľko minút a sú pozorované pri všetkých potenciálnych hodnotách. Zvýšenie zvodových prúdov K + vedie k hyperpolarizácii membrány, zatiaľ čo ich potlačenie vedie k depolarizácii. ...Existencia kanálového mechanizmu zodpovedného za zvodové prúdy však zostala dlho otázna. Až teraz sa ukázalo, že únik draslíka je prúd cez špeciálne draslíkové kanály.
Zefirov A.L. a Sitdiková G.F. Iónové kanály excitabilnej bunky (štruktúra, funkcia, patológia).
Od chemických až po elektrické
A teraz - ešte raz to najdôležitejšie. Z pohybu sa musíme vedome pohnúť chemické častice k pohybu elektrické náboje.
Draslík (K +) je kladne nabitý, a preto keď opustí bunku, odoberie z nej nielen seba, ale aj kladný náboj. Za ním z vnútra bunky k membráne sa tiahnu "mínusy" - záporné náboje. Ale nemôžu preniknúť cez membránu - na rozdiel od draselných iónov - pretože. neexistujú pre ne vhodné iónové kanály a membrána ich neprepustí. Pamätáte si na negativitu -60 mV, ktorú sme nevysvetlili? Toto je samotná časť pokojového membránového potenciálu, ktorý vzniká únikom iónov draslíka z bunky! A to je veľká časť oddychového potenciálu.
Pre túto zložku pokojového potenciálu existuje dokonca špeciálny názov – koncentračný potenciál. koncentračný potenciál - je to časť pokojového potenciálu, ktorý vzniká deficitom kladných nábojov vo vnútri bunky, ktorý vzniká únikom kladných iónov draslíka z bunky.
No a teraz trochu fyziky, chémie a matematiky pre milovníkov presnosti.
Elektrické sily súvisia s chemickými silami podľa Goldmanovej rovnice. Jeho konkrétnym prípadom je jednoduchšia Nernstova rovnica, ktorú možno použiť na výpočet rozdielu transmembránového difúzneho potenciálu na základe rôznych koncentrácií iónov rovnakého druhu na rôznych stranách membrány. Takže, keď poznáme koncentráciu draselných iónov vonku a vo vnútri bunky, môžeme vypočítať rovnovážny potenciál draslíka E K:

kde E k - rovnovážny potenciál, R je plyn konštantný, T je absolútna teplota, F- Faradayova konštanta, K + ext a K + ext - koncentrácie iónov K + mimo a vo vnútri bunky, resp. Vzorec ukazuje, že na výpočet potenciálu sa navzájom porovnávajú koncentrácie iónov rovnakého typu - K +.
Presnejšie, konečná hodnota celkového difúzneho potenciálu, ktorý vzniká únikom viacerých druhov iónov, sa vypočíta pomocou Goldman-Hodgkin-Katzovho vzorca. Berie do úvahy, že pokojový potenciál závisí od troch faktorov: (1) polarita elektrického náboja každého iónu; (2) priepustnosť membrány R pre každý ión; (3) [koncentrácie zodpovedajúcich iónov] vo vnútri (int) a mimo membrány (ex). Pre pokojovú membránu axónu chobotnice je pomer vodivosti R K: PNa :P Cl = 1:0,04:0,45.
Záver
Oddychový potenciál sa teda skladá z dvoch častí:
- -10 mV, ktoré sa získavajú „asymetrickou“ prevádzkou čerpadla membránového výmenníka (koniec koncov, odčerpáva z článku viac kladných nábojov (Na +), ako prečerpáva späť draslíkom).
- Druhou časťou je draslík, ktorý neustále uniká z bunky a odnáša kladné náboje. Jeho príspevok je hlavný: -60 mV. V súhrne to dáva požadovaných -70 mV.
Je zaujímavé, že draslík prestane opúšťať bunku (presnejšie, jeho vstup a výstup sa vyrovnajú) až pri hladine negativity bunky -90 mV. V tomto prípade sa chemické a elektrické sily vyrovnajú, pretlačia draslík cez membránu, ale nasmerujú ho opačným smerom. Tomu však bráni neustály únik sodíka do bunky, ktorý so sebou nesie kladné náboje a znižuje negativitu, o ktorú draslík „bojuje“. A v dôsledku toho sa v bunke udržiava rovnovážny stav na úrovni -70 mV.
Teraz je konečne vytvorený pokojový membránový potenciál.
Schéma Na+/K+-ATPázy jasne ilustruje "asymetrickú" výmenu Na + za K +: odčerpanie nadbytku "plus" v každom cykle operácie enzýmu vedie k negatívnemu náboju vnútorného povrchu membrány. Toto video nehovorí, že ATPáza je zodpovedná za menej ako 20 % pokojového potenciálu (-10 mV): zostávajúca „negativita“ (-60 mV) pochádza z opustenia bunky cez „kanály úniku draslíka“ K. ióny + , snažiac sa vyrovnať ich koncentráciu vo vnútri a mimo bunky.
Literatúra
- Jacqueline Fischer-Lougheed, Jian-Hui Liu, Estelle Espinos, David Mordasini, Charles R. Bader, et. kol., (2001). Fúzia ľudského myoblastu vyžaduje vyjadrenie funkčných kanálov Kir2.1 vnútorného usmerňovača. J Cell Biol. 153 , 677-686;
- Liu J.H., Bijlenga P., Fischer-Lougheed J. a kol. (1998). Úloha vnútorného usmerňovacieho K + prúdu a hyperpolarizácie vo fúzii ľudských myoblastov. J Physiol. 510 , 467–476;
- Sarah Sundelacruz, Michael Levin, David L. Kaplan. (2008). Membránový potenciál riadi adipogénnu a osteogénnu diferenciáciu mezenchymálnych kmeňových buniek. PLOS ONE. 3 e3737;
- Pavlovská M.V. a Mamykin A.I. Elektrostatika. Dielektrika a vodiče v elektrickom poli. Jednosmerný prúd / Elektronická príručka pre všeobecný kurz fyziky. Petrohrad: Štátna elektrotechnická univerzita v Petrohrade;
- Nozdrachev A.D., Bazhenov Yu.I., Barannikova I.A., Batuev A.S. a iné.Začiatky fyziológie: Učebnica pre stredné školy / Ed. akad. PEKLO. Nozdrachev. Petrohrad: Lan, 2001. - 1088 s.;
- Makarov A.M. a Luneva L.A. Základy elektromagnetizmu / Fyzika v technická univerzita. T. 3;
- Zefirov A.L. a Sitdiková G.F. Iónové kanály excitabilnej bunky (štruktúra, funkcia, patológia). Kazaň: Art-cafe, 2010. - 271 s.;
- Rodina T.G. Senzorická analýza potravinárskych výrobkov. Učebnica pre vysokoškolákov. M.: Akadémia, 2004. - 208 s.;
- Kolman J. a Rem K.-G. Vizuálna biochémia. M.: Mir, 2004. - 469 s.;
- Šulgovský V.V. Základy neurofyziológie: Návod pre vysokoškolákov. Moskva: Aspect Press, 2000. - 277 s.
História objavov
V roku 1902 Julius Bernstein predložil hypotézu, podľa ktorej bunková membrána umožňuje vstup iónov K + do bunky, ktoré sa hromadia v cytoplazme. Výpočet pokojového potenciálu podľa Nernstovej rovnice pre draslíkovú elektródu sa uspokojivo zhodoval s nameraným potenciálom medzi svalovou sarkoplazmou a okolím, ktorý bol asi - 70 mV.
Podľa teórie Yu.Bernshteina, keď je bunka excitovaná, jej membrána je poškodená a ióny K + vytekajú z bunky pozdĺž koncentračného gradientu, kým sa membránový potenciál nestane nulovým. Potom membrána obnoví svoju integritu a potenciál sa vráti na úroveň pokojového potenciálu. Toto tvrdenie, skôr akčný potenciál, vyvrátili Hodgkin a Huxley v roku 1939.
Bernsteinovu teóriu o pokojovom potenciáli potvrdil Kenneth Stewart Cole, niekedy sú jeho iniciály mylne napísané ako K.C. Cole, kvôli svojej prezývke, Casey ("Kacy"). PP a PD sú zobrazené na slávnej ilustrácii Colea a Curtisa z roku 1939. Táto kresba sa stala emblémom Membrane Biophysics Group Biophysical Society (pozri ilustráciu).
Všeobecné ustanovenia
Aby bol potenciálny rozdiel na membráne zachovaný, je potrebné, aby bol určitý rozdiel v koncentrácii rôznych iónov vnútri a mimo bunky.
Koncentrácie iónov v bunke kostrového svalstva a v extracelulárnom prostredí
Pokojový potenciál pre väčšinu neurónov je asi -60 mV - -70 mV. Bunky neexcitabilných tkanív majú tiež potenciálny rozdiel na membráne, ktorý je odlišný pre bunky rôznych tkanív a organizmov.
Tvorba pokojového potenciálu
PP sa tvorí v dvoch etapách.
Prvé štádium: vytvorenie zanedbateľnej (-10 mV) negativity vo vnútri bunky v dôsledku nerovnakej asymetrickej výmeny Na + za K + v pomere 3 : 2. Výsledkom je, že viac kladných nábojov opúšťa bunku so sodíkom, ako sa do nej vracia draslík. Táto vlastnosť sodíkovo-draslíkovej pumpy, ktorá vymieňa tieto ióny cez membránu s výdajom energie ATP, zabezpečuje jej elektrogenitu.
Výsledky činnosti membránových čerpadiel na výmenu iónov v prvej fáze tvorby PP sú nasledovné:
1. Nedostatok sodíkových iónov (Na +) v bunke.
2. Nadbytok draselných iónov (K +) v bunke.
3. Výskyt slabého elektrického potenciálu na membráne (-10 mV).
Druhá fáza: vytvorenie výraznej (-60 mV) negativity vo vnútri bunky v dôsledku úniku iónov K + z nej cez membránu. Draselné ióny K + opúšťajú bunku a odoberajú z nej kladný náboj, čím záporný náboj dosahuje -70 mV.
Pokojový membránový potenciál je teda deficit kladných elektrických nábojov vo vnútri bunky, ku ktorému dochádza v dôsledku úniku kladných iónov draslíka z bunky a elektrogénneho pôsobenia sodíkovo-draselnej pumpy.
pozri tiež
Poznámky
Odkazy
Dudel J., Ruegg J., Schmidt R. a kol. Fyziológia človeka: v 3 zväzkoch. Za. z angličtiny / upravili R. Schmidt a G. Thevs. - 3. - M .: Mir, 2007. - T. 1. - 323 s ilustráciami. s - 1500 kópií. - ISBN 5-03-000575-3
Nadácia Wikimedia. 2010.
Pozrite sa, čo je „potenciál odpočinku“ v iných slovníkoch:
KLIDOVÝ POTENCIÁL, elektrický potenciál medzi vnútorným a vonkajším prostredím bunky, vznikajúci na jej membráne; v neurónoch a svalových bunkách dosahuje hodnotu 0,05 0,09 V; vzniká nerovnomernou distribúciou a akumuláciou iónov v rôznych ... encyklopedický slovník
Pokojový membránový potenciál, potenciálny rozdiel, ktorý existuje v živých bunkách v stave fiziol. pokoj, medzi ich cytoplazmou a extracelulárnou tekutinou. V nervových a svalových bunkách sa P. p. zvyčajne pohybuje v rozmedzí 60-90 mV a ext. strana…
oddychový potenciál- pokojový stres - [Ya.N. Luginsky, M.S. Fezi Zhilinskaya, Yu.S. Kabirov. Anglický ruský slovník elektrotechniky a energetiky, Moskva, 1999] Elektrotechnické témy, základné pojmy Synonymá pokojové napätie EN pokojový potenciálresting ... ... Technická príručka prekladateľa
oddychový potenciál- Odpočinkový potenciál Potenciál, ktorý existuje medzi prostredím, v ktorom sa bunka nachádza, a jej obsahom... Výkladový anglicko-ruský slovník nanotechnológie. - M.
oddychový potenciál- Potenciál neaktívneho neurónu. Tiež sa nazýva membránový potenciál... Psychológia vnemov: glosár
oddychový potenciál- potenciálny rozdiel medzi obsahom bunky a extracelulárnou tekutinou. V nervových bunkách p.p. podieľa sa na udržiavaní pripravenosti bunky na excitáciu. * * * Membránový bioelektrický potenciál (asi 70 mV) v nervovej bunke umiestnenej v ... ... Encyklopedický slovník psychológie a pedagogiky
oddychový potenciál- - rozdiel v elektrických nábojoch medzi vonkajším a vnútorným povrchom membrány v stave fyziologického zvyšku bunky, zaznamenaný pred začiatkom stimulu ... Slovník pojmov pre fyziológiu hospodárskych zvierat
Membránový potenciál zaznamenaný pred začiatkom stimulu ... Veľký lekársky slovník
- (fyziologický) potenciálny rozdiel medzi obsahom bunky (vláknami) a extracelulárnou tekutinou; potenciálny skok je lokalizovaný na povrchovej membráne, pričom jej vnútorná strana sa nabíja elektronegatívne vzhľadom na ... ... Veľká sovietska encyklopédia
Rýchla fluktuácia (špička) membránového potenciálu, ku ktorej dochádza pri excitácii nervových, svalových, niektorých žľazových a rastových buniek; elektrický signál, ktorý zabezpečuje rýchly prenos informácií v tele. Riadi sa pravidlom všetko alebo nič... Biologický encyklopedický slovník
knihy
- 100 spôsobov, ako zmeniť svoj život. Časť 1, Larisa Parfentyeva. O knihe Zbierka inšpiratívnych príbehov o tom, ako zmeniť svoj život k lepšiemu, od muža, ktorý dokázal zmeniť svoj vlastný život 180 stupňov. Táto kniha sa zrodila z týždenného stĺpca...