Proprietăți chimice. Glicina și sarea sa de sodiu (E640) Proprietățile chimice ale aminoacizilor
Care îndeplinește funcții biologice importante în organismele vii, participă la biosinteza proteinelor, este responsabil pentru activitatea normală a sistemului nervos și reglează procesele metabolice. Acidul aminoacetic, derivat artificial, este utilizat în produse farmaceutice, medicină și industria alimentară.
Aditivul alimentar E640 combină sub un număr de etichetare acidul aminoacetic (glicină) și sarea sa de sodiu - compuși care sunt utilizați pentru a optimiza gustul și aroma produselor. Suplimentul este sigur și aprobat oficial în majoritatea țărilor lumii.
Glicina și sarea sa de sodiu: informații generale
Glicina, cunoscută și ca acid aminoacetic sau aminoetanoic, aparține unui număr de aminoacizi neesențiali - cele mai simple structuri organice care fac parte din proteine și compușii acestora. Substanța, obținută artificial, este o pulbere incoloră, inodoră și are un gust dulceag.
La scară industrială, glicina este produsă prin combinarea acidului cloracetic și a amoniacului. Acidul aminoacetic, la rândul său, are proprietatea de a forma săruri complexe (glicinați) cu ionii metalici.
Glicinatul de sodiu este o sare de sodiu și acid aminoacetic, care este și o substanță de origine sintetică. În ciuda faptului că glicina și sarea ei sunt compuși chimici diferiți, în industria alimentară ele îndeplinesc funcții identice ca modificatorii de gust și aromă, sunt combinate sub un număr de etichetă și sunt considerate ca aditiv E640.
| Nume | Glicina |
|---|---|
| Sinonime | Acid aminoacetic (aminoetanoic), glicocol (învechit) |
| grup | Aminoacizi neesențiali |
| Formula chimica | NH 2 – CH 2 – COOH |
| Structura | Cristale monoclinice fine (pulbere cristalină) |
| Culoare | Alb (incolor) |
| Miros | Absent |
| Gust | Dulce |
| Solubilitate | Complet solubil în, parțial solubil în. Nu se dizolvă în eter |
| Cod aditiv | E640 (inclusiv sare de sodiu) |
| Origine | Sintetic |
| Toxicitate | Sigur atunci când este consumat în limite normale |
| Domenii de utilizare | Industria alimentară, farmaceutică, medicină, cosmetologie |
Rolul biologic al glicinei și sursele sale
Glicina se găsește în moleculele proteice mult mai des decât alți aminoacizi și îndeplinește funcții biologice importante. În corpul uman, acest aminoacid este sintetizat prin transaminarea (transferul reversibil al grupării amino) de glioxilat sau scindarea enzimatică a colinei și serinei.
Acidul aminoacetic este un precursor al porfirinelor și purinelor, a căror biosinteză are loc în celulele vii, dar rolul biologic al acestui compus nu se limitează la aceste funcții. Glicina este, de asemenea, un neurotransmițător care este implicat în transmiterea impulsurilor nervoase, reglează producția de alți aminoacizi și are un efect „inhibitor” asupra neuronilor și neuronilor motori.
Corpul unei persoane sănătoase sintetizează în mod independent aminoacizii în cantitățile necesare, așa că, de regulă, nu este nevoie de utilizarea lor în medicamente și suplimente alimentare. Sursele alimentare de acid aminoacetic includ produsele de origine animală (ficatul de vită), nucile și unele fructe.
Efectul glicinei și al sării sale de sodiu asupra corpului uman
Acidul aminoacetic ca neurotransmițător îndeplinește funcții de reglare și afectează în primul rând sistemul nervos central și periferic. Glicina are proprietăți nootrope, normalizează metabolismul, activează funcțiile de protecție ale sistemului nervos central și are un efect calmant ușor.
Efectele pozitive ale glicinei asupra corpului uman:
- reducerea tensiunii emoționale, anxietății, stresului, agresivității;
- starea de spirit îmbunătățită și normalizarea somnului;
- relaxarea mușchilor și ameliorarea crampelor;
- performanță crescută;
- reducerea efectelor secundare ale consumului de medicamente psihotrope;
- reducerea severității tulburărilor vegetativ-vasculare;
- reducerea poftelor de alcool și dulciuri.
Ca parte a suplimentului E640, glicina și sarea ei nu au proprietățile de mai sus și nu au efecte nici pozitive, nici negative asupra organismului uman atunci când sunt consumate în limite normale. Aditivul alimentar nu reprezintă o amenințare pentru sănătate, dar în caz de intoleranță individuală poate provoca o reacție alergică.
Potențiale pericole pot proveni din impuritățile din aditiv și din produsele alimentare de calitate scăzută, în fabricarea cărora se folosesc optimizatori de gust și aromă.
Aplicarea glicinei și a sării sale de sodiu
Aplicațiile glicinei și glicinatului de sodiu sunt limitate în principal la industria alimentară, medicamente și produse farmaceutice. Cu toate acestea, acidul aminoacetic și-a găsit aplicație și în industria cosmetică datorită hipoalergenicității și efectului antioxidant.
Cosmetice care conțin aditivul E640:
- șampoane medicamentoase pentru păr slăbit și produse anti-chelie;
- cosmetice anti-îmbătrânire, creme hidratante și măști pentru toate tipurile de piele;
- seruri și toner de curățare;
- rujuri si balsamuri.
Tabletele de glicină zdrobite pot fi folosite pentru a face produse de îngrijire a pielii de casă și adăugate la măștile și cremele hidratante. Acidul aminoacetic promovează pătrunderea componentelor nutritive valoroase în straturile profunde ale dermei și sporește efectul cosmeticelor medicinale.
Aditiv E640 în industria alimentară
 Glicina și glicinatul de sodiu sunt utilizate în mod activ în procesele tehnologice de producere a băuturilor alcoolice. Aditivul E640, în special, este inclus în vodca de elită, care ajută la neutralizarea mirosului neplăcut și atenuează gustul dur. Există, de asemenea, opinia că prezența glicinei în băuturile alcoolice ajută la reducerea efectului toxic al alcoolului asupra sistemului nervos și previne mahmureala.
Glicina și glicinatul de sodiu sunt utilizate în mod activ în procesele tehnologice de producere a băuturilor alcoolice. Aditivul E640, în special, este inclus în vodca de elită, care ajută la neutralizarea mirosului neplăcut și atenuează gustul dur. Există, de asemenea, opinia că prezența glicinei în băuturile alcoolice ajută la reducerea efectului toxic al alcoolului asupra sistemului nervos și previne mahmureala.
Produse alimentare care conțin aditivul E640:
- băuturi alcoolice tari;
- gemuri, conserve, jeleuri, ;
- sucuri ambalate cu pulpă;
- gătit îmbogățit;
- băuturi vitaminice pentru sport;
- sosuri, condimente și condimente.
Acidul aminoacetic este folosit nu numai pentru a optimiza gustul și transportul substanțelor biologic active, ci și ca agent antibacterian. În special, este folosit pentru a trata carnea, peștele și fructele de mare pentru a neutraliza E. coli periculoasă.
Uz medical
Glicina este utilizată în mod activ pentru tratamentul și prevenirea bolilor asociate cu sistemul nervos central și periferic. Această substanță face parte din preparatele farmaceutice cu efecte nootrope, sedative, anticonvulsivante și hipnotice și are un efect ușor antidepresiv și tranchilizant.
Indicații medicale pentru utilizarea acidului aminoacetic ca medicament:
- scăderea performanței mentale, tulburări de somn și memorie;
- tensiune emoțională, situații stresante, nevroze;
- instabilitate emoțională și excitabilitate crescută;
- consecințele accidentului vascular cerebral ischemic, leziunilor cerebrale traumatice și neuroinfecțiilor;
- distonie vegetativ-vasculară, ischemie;
- tonus muscular crescut, crampe musculare;
- dependența de alcool și droguri, efecte toxice ale medicamentelor care deprimă sistemul nervos central.
S-a dovedit că consumul a 3 g de glicină pe zi are un efect pozitiv asupra abilităților mentale și asupra stării emoționale generale a unei persoane, ameliorează somnolența în timpul zilei și normalizează somnul nocturn. De asemenea, medicamentul este prescris femeilor însărcinate pentru a reduce anxietatea, copiilor și adolescenților care întâmpină dificultăți de adaptare socială și de concentrare.
Aditiv E640 și legislație
Optimizatorul de gust și miros E640 este utilizat în producția de alimente în majoritatea țărilor lumii, dar nu există informații despre aditiv în Codex Alimentarius. Nu au existat cazuri de intoxicație cu glicina și glicinat de sodiu atunci când sunt consumate ca aliment, așa că modificatorul E640 este considerat sigur.
Aditivul este inclus în lista produselor aprobate oficial pentru utilizare în industria alimentară din Uniunea Europeană, SUA și Canada. Legislația Federației Ruse și a Belarusului permite, de asemenea, prezența E640 în produse în limitele permise stabilite de SanPiN. Nu există date despre utilizarea E640 ca potențiator de aromă și agent de aromatizare în Ucraina.
În ciuda faptului că glicina și sarea ei nu au un efect toxic asupra corpului uman și sunt aprobate pentru utilizare, produsele care conțin E640 cu greu pot fi numite utile. Majoritatea aromelor și aromelor sunt folosite pentru a atrage atenția cumpărătorului asupra produselor de calitate scăzută, a căror utilizare ar trebui redusă la minimum.
Proteinele sunt polipeptide cu o greutate moleculară destul de mare care au o anumită structură spațială, care depinde de secvența de aminoacizi incluși în lanțul proteic. Această structură poate fi compactă (proteine globulare) sau alungită (proteine fibrilare). Toate enzimele sunt proteine globulare, proteinele fibrilare includ colagenul, keratina - proteine ale pielii și părului, foarte puternice și foarte extensibile.
Pe baza compoziției lor, proteinele sunt împărțite în simple, constând numai din aminoacizi și complexe - complexe sau compuși covalenti ai polipeptidelor cu molecule din alte clase:
acizi nucleici – nucleoproteine;
polizaharide – glicoproteine;
lipide – lipoproteine;
pigmenți – cromoproteine;
reziduuri de acid fosforic - fosfoproteine.
Partea proteică a unei proteine complexe se numește apobelcom, neprotein - grupare prostetică. Aproape toate proteinele globulare simple și complexe sunt enzime - catalizatori biologici ai reacțiilor biochimice în organismele vii.
Sarcini
Sarcina 1. Ce volum de gaz (în condiţii normale) va fi eliberat când 0,001 mol de aminoacid reacţionează cu acidul azot: a) leucina; b) lizina; c) prolina?
Soluţie
Să notăm ecuațiile pentru reacțiile aminoacizilor enumerați cu acidul azot. În cazul leucinei și lizinei, deaminarea are loc conform lui Van Slyke, iar pentru lizină - pe două grupări amino conținute în moleculă. Prolina nu are o grupare amino primară, așa că procesul se oprește în stadiul de N-nitrozare.
În reacția (a), numărul de moli de leucină n(Leu) este egal cu numărul de moli de azot eliberat n(N2), deci se eliberează 0,001 mol sau 22,4 ml de azot. În reacția (b) se formează o cantitate dublă de gaz 2n(N2) comparativ cu n(lys), deoarece aminoacidul original are două grupări amino primare; volumul de azot eliberat va fi de 44,8 ml. În reacția (c), azotul nu este eliberat: prolina este singurul dintre cei 20 de aminoacizi esențiali care are un atom secundar de azot în poziția a. Când este nitrosat, se formează un compus N-nitrozo (mai degrabă decât diazo).
Răspuns: a) 22,4 ml N2; b) 44,8 ml N2; c) nu există eliberare de N2.
Sarcina 2. Ca rezultat al tratării unei soluții care conține 9,36 mg dintr-un aminoacid necunoscut cu un exces de acid azot la 748 mm Hg. şi 20°C, s-au obţinut 2,01 ml de azot. Care este masa molară minimă a acestui aminoacid?
Soluţie
Reacția aminoacidului cu acidul azot:

Folosind legea combinată a gazelor PV/T = const, să calculăm volumul de azot în condiții normale (la o temperatură de 0 ° C, sau 273 ° K și o presiune de 760 mm Hg): V 0 (N 2) (n.s.) = (P 1 · V 1 · T0)/(P0.T1) = (748.2.01.273)/(760.293) = 1.84 ml.
Deoarece numărul de moli ai substanței aminoacide și gazul degajat N2 sunt același, vom face proporția:
9,36 mg de aminoacid dau 1,84 ml de N2;
M (greutatea moleculară a aminoacidului) va da = 22,4 N 2.
M = (9,36.22,4)/1,84 = 114.
Ar putea fi valina: 
Sarcina 3. Hemoglobina animală conține 0,335% fier (în greutate). Care este masa molară minimă a acestei proteine? Câți atomi de fier sunt incluși în moleculă dacă greutatea moleculară a proteinei, determinată prin măsurarea presiunii osmotice, este de 67.000?
Soluţie
Fracția de masă a fierului din hemoglobină: C%(Fe) = /M(proteină), unde n este numărul de atomi de Fe din molecula proteică. Fie n = 1, atunci M(proteină)1 = M(Fe) 100%/C%(Fe) = 56 100/0,335 = 16700. Deoarece valoarea adevărată (prin condiție) a sursei M(proteine). = 67000, n = M sursă/M 1 = 67000/16700 = 4.
Sarcina 4.În timpul hidrolizei alcaline a 48 g dintr-o dipeptidă constând din reziduuri ale aceluiași aminoacid, s-a format o singură substanță - sarea de sodiu a aminoacidului. Masa acestei sări este de 66,6 g. Stabiliți structura dipeptidei.
Soluţie
Ecuația de reacție pentru hidroliza alcalină a dipeptidei:
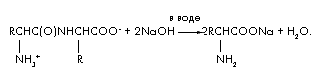
Să notăm cantitatea de dipeptidă în moli (dipeptidă) = x. Apoi reacția de hidroliză consumă de două ori cantitatea de alcali (NaOH) = 2x și produce (aminoacizi) = 2x și (H2O) = x. Să creăm o ecuație de bilanț al materialelor folosind formula m = ·M;
m(dipeptidă) + m(NaOH) = m(săruri de aminoacizi) + m(H20); 48 + 2x 40 = 66,6 + x 18; 62x = 18,6; x = 0,3 mol. M(dipeptidă) = m/ = 48/0,3 = 160. M(aminoacizi) = [M(dipeptidă) + M(H20)]/2 = 178/2 = 89 g/mol. Aminoacidul este alanina. Structura dipeptidei: ![]() .
.
Glicina (acid aminoacetic, glicocol, Gly, G)
H2NCH2COOH
Masa moleculara 75,07; cristale incolore; t se topeste 232-236°С (cu descompunere); foarte solubil în apă, insolubil în majoritatea solvenților organici. La 25°C p K a 2,34 (COOH) şi 9,6 (NH2); R eu 5,97.
În ceea ce privește proprietățile chimice, glicina este un α-aminoacid alifatic tipic. Determinarea cantitativă se bazează pe formarea de produse colorate cu o-ftalaldehidă (reacția Zimmermann). Se găsește mai des în proteine decât în alți aminoacizi. Servește ca precursor în biosinteza compușilor porfirine și a bazelor purinice. Glicina este un aminoacid codificat, neesențial; biosinteza sa se realizează prin transaminarea acidului glioxilic, scindarea enzimatică a serinei și treoninei. Licina este sintetizată din acid cloracetic și NH3. În spectrul RMN în D2O, deplasarea chimică a protonilor din grupa CH2 este de 3,55 ppm. Sarea internă a glicinei (CH 3) 3 + NCH 2 COO se numește betaină.
Glicina este utilizată pentru sinteza peptidelor, ca componentă a soluțiilor tampon, în amestec cu alți aminoacizi - pentru nutriția parenterală.
Cromatogramele probelor care conțin această substanță
Proprietățile aminoacizilor pot fi împărțite în două grupe: chimice și fizice.
Proprietățile chimice ale aminoacizilor
În funcție de compuși, aminoacizii pot prezenta proprietăți diferite.
Interacțiuni cu aminoacizi:
Aminoacizii, ca compuși amfoteri, formează săruri atât cu acizii, cât și cu alcalii.
Ca acizi carboxilici, aminoacizii formează derivați funcționali: săruri, esteri, amide.
Interacțiunea și proprietățile aminoacizilor cu motive:
Se formează săruri:
NH2-CH2-COOH + NaOH NH2-CH2-COONa + H2O
Sare de sodiu + acid 2-aminoacetic Sare de sodiu a acidului aminoacetic (glicină) + apă
Interacțiunea cu alcooli:
Aminoacizii pot reacționa cu alcoolii în prezența gazului clorhidric, transformându-se în ester. Esterii de aminoacizi nu au o structură bipolară și sunt compuși volatili.
NH2-CH2-COOH + CH3OH NH2-CH2-COOCH3 + H2O.
Ester metilic / acid 2-aminoacetic /
Interacţiune amoniac:
Se formează amide:
NH2-CH(R)-COOH + H-NH2 = NH2-CH(R)-CONH2 + H20
Interacțiunea aminoacizilor cu acizi tari:
Primim săruri:
HOOC-CH 2 -NH 2 + HCl → Cl (sau HOOC-CH 2 -NH 2 *HCl)
Acestea sunt proprietățile chimice de bază ale aminoacizilor.
Proprietățile fizice ale aminoacizilor
Să enumerăm proprietățile fizice ale aminoacizilor:
- Incolor
- Au o formă cristalină
- Majoritatea aminoacizilor au un gust dulce, dar in functie de radical (R), pot fi amari sau fara gust.
- Ușor solubil în apă, dar slab solubil în mulți solvenți organici
- Aminoacizii au proprietatea de activitate optică
- Se topește cu descompunere la temperaturi peste 200°C
- Ne volatil
- Soluțiile apoase de aminoacizi în medii acide și alcaline conduc curentul electric

Aminoacizii conțin grupări amino și carboxil și prezintă toate proprietățile caracteristice compușilor cu astfel de grupări funcționale. La scrierea reacțiilor cu aminoacizi, se folosesc formule cu grupări amino și carboxi neionizate.
1) reacții la grupa amino. Gruparea amino din aminoacizi prezintă proprietățile obișnuite ale aminelor: aminele sunt baze și acționează ca nucleofile în reacții.
1. Reacția aminoacizilor ca baze. Când aminoacizii interacționează cu acizii, se formează săruri de amoniu:
clorhidrat de glicină, sare clorhidrat de glicină
2. Acțiunea acidului azotat. Când acidul azot acționează, se formează hidroxiacizi și se eliberează azot și apă:
Această reacție este utilizată pentru determinarea cantitativă a grupărilor de amine libere din aminoacizi, precum și din proteine.
3. Formarea derivaților N - acil, reacția de acilare.
Aminoacizii reacţionează cu anhidride şi halogenuri acide, formând derivaţi N - acil ai aminoacizilor:
Benzil eter sare de sodiu N carbobenzoxiglicina - glicina cloroformică
Acilarea este una dintre modalitățile de a proteja gruparea amino. Derivații de N-acil sunt de mare importanță în sinteza peptidelor, deoarece derivații de N-acil sunt ușor hidrolizați pentru a forma o grupare amino liberă.
4. Formarea bazelor Schiff. Când a-aminoacizii interacționează cu aldehidele, iminele substituite (bazele Schiff) se formează prin etapa de formare a carbinolaminelor:
alanin formaldehida N-metilol derivat al alaninei
5. Reacția de alchilare. Gruparea amino din a-aminoacidul este alchilată pentru a forma derivați N-alchil:
Reacția cu 2,4-dinitrofluorobenzen este de cea mai mare importanță. Derivații de dinitrofenil rezultați (derivați DNP) sunt utilizați la stabilirea secvenței de aminoacizi a peptidelor și proteinelor. Interacțiunea a-aminoacizilor cu 2,4-dinitrofluorobenzen este un exemplu de reacție de substituție nucleofilă în ciclul benzenic. Datorită prezenței a două grupări puternice de atragere de electroni în inelul benzenic, halogenul devine mobil și suferă o reacție de substituție:
 |
2.4 – dinitro -
fluorobenzen N - 2,4 - dinitrofenil - a - aminoacid
(DNPB) DNP - derivați ai a - aminoacizilor
6.Reacția cu izotiocianat de fenil. Această reacție este utilizată pe scară largă în determinarea structurii peptidelor. Izotiocianatul de fenil este un derivat al acidului izotiocianic H-N=C=S. Interacțiunea a-aminoacizilor cu izotiocianatul de fenil are loc prin mecanismul unei reacții de adiție nucleofilă. Produsul rezultat suferă apoi o reacție de substituție intramoleculară, conducând la formarea unei amide substituite ciclice: feniltiohidantoina.
Compușii ciclici se obțin cu randament cantitativ și sunt derivați fenil ai tiohidantoinei (derivați PTH) - aminoacizi. Derivații PTG diferă în structura radicalului R.
Pe lângă sărurile obișnuite, a-aminoacizii pot forma, în anumite condiții, săruri intracomplexe cu cationi de metale grele. Toți a-aminoacizii sunt caracterizați prin săruri de cupru intracomplex (chelate) cu cristalizare minunată, de culoare intens albastru:
Ester etilic al alaninei
Formarea esterilor este una dintre metodele de protejare a grupării carboxil în sinteza peptidelor.
3. Formarea halogenurilor acide. Când acționează asupra a-aminoacizilor cu o grupare amino protejată cu oxidiclorura de sulf (clorura de tionil) sau triclorura de oxid de fosfor (oxiclorura de fosfor), se formează cloruri acide:
Producția de halogenuri acide este una dintre modalitățile de activare a grupării carboxil în sinteza peptidelor.
4.Obținerea anhidridelor de a-aminoacizi. Halogenurile acide sunt foarte reactive, ceea ce reduce selectivitatea reacției atunci când sunt utilizate. Prin urmare, o metodă mai frecvent utilizată pentru activarea unei grupări carboxil în sinteza peptidelor este transformarea acesteia într-o grupare anhidridă. Anhidridele sunt mai puțin active decât halogenurile acide. Când un a-aminoacid cu o grupare amino protejată interacționează cu acidul etil cloroformic (cloroformiat de etil), se formează o legătură anhidridă:
5. Decarboxilarea. a - Aminoacizii care au două grupări atrăgătoare de electroni la același atom de carbon sunt ușor decarboxilați. În condiții de laborator, aceasta se realizează prin încălzirea aminoacizilor cu hidroxid de bariu. Această reacție are loc în organism cu participarea enzimelor decarboxilaze cu formarea de amine biogene:
ninhidrina
Relația aminoacizilor cu căldura. Când a-aminoacizii sunt încălziți, se formează amide ciclice numite dicetopiperazine:

Diketopiperazina
g - și d - Aminoacizii desprind ușor apa și se ciclează pentru a forma amide interne, lactame:
g - lactam (butirolactamă)
În cazurile în care grupările amino și carboxil sunt separate de cinci sau mai mulți atomi de carbon, atunci când sunt încălzite, are loc policondensarea cu formarea de lanțuri de poliamidă polimerică cu eliminarea unei molecule de apă.





