Получение железа высокой чистоты. Решение химических задач на закон фарадея в курсе средней школы Теоретические сведения по проблеме
Решение химических задач
на закон Фарадея в курсе
средней школы
Авторская разработка
Среди великого множества разнообразных
химических задач, как показывает практика
преподавания в школе, наибольшие затруднения
вызывают задачи, для решения которых помимо
прочных химических знаний требуется неплохо
владеть материалом курса физики. И хотя далеко не
в каждой средней школе уделяется внимание
решению хотя бы простейших задач с
использованием знаний двух курсов – химии и
физики, задачи такого типа иногда встречаются на
вступительных экзаменах в вузах, где химия
является профилирующей дисциплиной. А потому, не
разобрав задачи такого типа на уроках, учитель
может неумышленно лишить своего ученика шанса на
поступление в вуз на химическую специальность.
Эта авторская разработка содержит свыше
двадцати задач, так или иначе связанных с темой
«Электролиз». Для решения задач данного типа
необходимо не только хорошо знать тему
«Электролиз» школьного курса химии, но и знать
закон Фарадея, который изучается в школьном
курсе физики.
Возможно, эта подборка задач не будет интересна
абсолютно всем ученикам в классе или всем
доступна. Тем не менее задачи данного типа
рекомендуется разобрать с группой
заинтересованных учащихся на кружковом или
факультативном занятии. Можно с уверенностью
отметить, что задачи такого типа усложненные и по
крайней мере не являются типовыми для школьного
курса химии (речь идет о средней
общеобразовательной школе), а потому задачи
данного типа можно смело включать в варианты
школьной или районной химической олимпиады для
10-х или 11-х классов.
Наличие подробного решения для каждой задачи
делает разработку ценным подспорьем, особенно
для начинающих учителей. Разобрав несколько
задач с учащимися на факультативном занятии или
занятии кружка, творчески работающий учитель
непременно задаст несколько однотипных задач на
дом и воспользуется данной разработкой в
процессе проверки домашних заданий, что позволит
существенно сэкономить бесценное учительское
время.
Теоретические сведения по проблеме
Химические реакции, протекающие под действием электрического тока на электродах, помещенных в раствор или расплав электролита, называют электролизом. Рассмотрим пример.
В стаканчике при температуре около 700 °С находится расплав хлорида натрия NaCl, в него погружены электроды. До пропускания через расплав электрического тока ионы Na + и Cl – движутся хаотически, однако при наложении электрического тока движение этих частиц становится упорядоченным: ионы Na + устремляются к отрицательно заряженному электроду, а ионы Cl – – к положительно заряженному электроду.
Ион – заряженный атом или группа атомов, обладающая зарядом.
Катион – положительно заряженный ион.
Анион – отрицательно заряженный ион.
Катод – отрицательно заряженный электрод (к нему движутся положительно заряженные ионы – катионы).
Анод – положительно заряженный электрод (к нему движутся отрицательно заряженные ионы – анионы).
Электролиз расплава хлорида натрия на платиновых электродах

Суммарная реакция:
![]()
Электролиз водного раствора хлорида натрия на угольных электродах

Суммарная реакция:
или в молекулярной форме:
Электролиз водного раствора хлорида меди(II) на угольных электродах
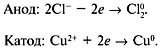
Суммарная реакция:
![]()
В электрохимическом ряду активности металлов медь расположена правее водорода, поэтому медь и будет восстанавливаться на катоде, а на аноде будет окисляться хлор.
Электролиз водного раствора сульфата натрия на платиновых электродах

Суммарная реакция:
![]()
Аналогично происходит электролиз водного раствора нитрата калия (платиновые электроды).
Электролиз водного раствора сульфата цинка на графитовых электродах

Суммарная реакция:
Электролиз водного раствора нитрата железа(III) на платиновых электродах

Суммарная реакция:
Электролиз водного раствора нитрата серебра на платиновых электродах

Суммарная реакция:
Электролиз водного раствора сульфата алюминия на платиновых электродах

Суммарная реакция:
Электролиз водного раствора сульфата меди на медных электродах – электрохимическое рафинирование

Концентрация CuSO 4 в растворе остается постоянной, процесс сводится к переносу материала анода на катод. В этом и заключается сущность процесса электрохимического рафинирования (получение чистого металла).
При составлении схем электролиза той или иной соли нужно помнить, что:
– катионы металлов, имеющие больший стандартный электродный потенциал (СЭП), чем у водорода (от меди до золота включительно), при электролизе практически полностью восстанавливаются на катоде;
– катионы металлов с небольшими значениями СЭП (от лития до алюминия включительно) не восстанавливаются на катоде, а вместо них восстанавливаются молекулы воды до водорода;
– катионы металлов, у которых значения СЭП меньше, чем у водорода, но больше, чем у алюминия (от алюминия до водорода), при электролизе на катоде восстанавливаются одновременно с водой;
– если водный раствор содержит смесь катионов различных металлов, например Ag + , Cu 2+ , Fe 2+ , то в этой смеси первым восстановится серебро, затем медь и последним – железо;
– на нерастворимом аноде в процессе электролиза происходит окисление анионов или молекул воды, причем анионы S 2– , I – , Br – , Cl – окисляются легко;
– если в растворе находятся анионы кислородсодержащих кислот , , , , то на аноде окисляются молекулы воды до кислорода;
– если анод растворим, то при электролизе он сам подвергается окислению, т. е. посылает электроны во внешнюю цепь: при отдаче электронов смещается равновесие между электродом и раствором и анод растворяется.
Если из всего ряда электродных процессов выделить только те, которые отвечают общему уравнению
М z + + ze = M,
то получим ряд напряжений металлов . В этот ряд всегда помещают также водород, что позволяет видеть, какие металлы способны вытеснять водород из водных растворов кислот, а какие нет (табл.).
Таблица
Ряд напряжений металлов
| Уравнение электродного процесса |
Стандартный электродный потенциал при 25 °С, В |
Уравнение электродного процесса |
Стандартный электродный потенциал при 25 °С, В |
|---|---|---|---|
| Li + + 1e = Li 0 | –3,045 | Co 2+ + 2e = Co 0 | –0,277 |
| Rb + + 1e = Rb 0 | –2,925 | Ni 2+ + 2e = Ni 0 | –0,250 |
| K + + 1e = K 0 | –2,925 | Sn 2+ + 2e = Sn 0 | –0,136 |
| Cs + + 1e = Cs 0 | –2,923 | Pb 2+ + 2e = Pb 0 | –0,126 |
| Ca 2+ + 2e = Ca 0 | –2,866 | Fe 3+ + 3e = Fe 0 | –0,036 |
| Na + + 1e = Na 0 | –2,714 | 2H + + 2e = H 2 | 0 |
| Mg 2+ + 2e = Mg 0 | –2,363 | Bi 3+ + 3e = Bi 0 | 0,215 |
| Al 3+ + 3e = Al 0 | –1,662 | Cu 2+ + 2e = Cu 0 | 0,337 |
| Ti 2+ + 2e = Ti 0 | –1,628 | Cu + +1e = Cu 0 | 0,521 |
| Mn 2+ + 2e = Mn 0 | –1,180 | Hg 2 2+ + 2e = 2Hg 0 | 0,788 |
| Cr 2+ + 2e = Cr 0 | –0,913 | Ag + + 1e = Ag 0 | 0,799 |
| Zn 2+ + 2e = Zn 0 | –0,763 | Hg 2+ + 2e = Hg 0 | 0,854 |
| Cr 3+ + 3e = Cr 0 | –0,744 | Pt 2+ + 2e = Pt 0 | 1,2 |
| Fe 2+ + 2e = Fe 0 | –0,440 | Au 3+ + 3e = Au 0 | 1,498 |
| Cd 2+ + 2e = Cd 0 | –0,403 | Au + + 1e = Au 0 | 1,691 |
В более простом виде ряд напряжений металлов можно представить так:
Для решения большинства задач на электролиз требуется знание закона Фарадея, формульное выражение которого приведено ниже:
m = M I t /(z F ),
где m – масса выделившегося на электроде вещества, F – число Фарадея, равное 96 485 А с/моль, или 26,8 А ч/моль, М – молярная масса элемента, восстанавливающегося в процессе электролиза, t – время проведения процесса электролиза (в секундах), I – сила тока (в амперах), z – число электронов, участвующих в процессе.
Условия задач
1. Какая масса никеля выделится в процессе электролиза раствора нитрата никеля в течение 1 ч при силе тока 20 А?
2. При какой силе тока необходимо проводить процесс электролиза раствора нитрата серебра, чтобы в течение 10 ч получить 0,005 кг чистого металла?
3. Какая масса меди выделится при электролизе расплава хлорида меди(II) в течение 2 ч при силе тока 50 А?
4. В течение какого времени нужно проводить процесс электролиза водного раствора сульфата цинка при силе тока 120 А, чтобы при этом получить 3,5 г цинка?
5. Какая масса железа выделится в процессе электролиза раствора сульфата железа(III) при силе тока 200 А в течение 2 ч?
6. При какой силе тока необходимо проводить процесс электролиза раствора нитрата меди(II), чтобы в течение 15 ч получить 200 г чистого металла?
7. В течение какого времени необходимо проводить процесс электролиза расплава хлорида железа(II) при силе тока 30 А, чтобы при этом получить 20 г чистого железа?
8. При какой силе тока необходимо проводить процесс электролиза раствора нитрата ртути(II), чтобы в течение 1,5 ч получить 0,5 кг чистого металла?
9. При какой силе тока необходимо проводить процесс электролиза расплава хлорида натрия, чтобы в течение 1,5 ч получить 100 г чистого металла?
10. Расплав хлорида калия подвергли электролизу в течение 2 ч при силе тока 5 А. Полученный металл прореагировал с водой массой 2 кг. Какой концентрации раствор щелочи получился при этом?
11.
Сколько граммов 30%-го раствора
соляной кислоты потребуется для полного
взаимодействия с железом, полученным при
электролизе раствора сульфата железа(III) в
течение 0,5 ч при силе тока
10 А?
12. В процессе электролиза расплава хлорида алюминия, проводимого в течение 245 мин при силе тока 15 А, получили чистый алюминий. Сколько граммов железа можно получить алюминотермическим методом при взаимодействии данной массы алюминия с оксидом железа(III)?
13. Сколько миллилитров 12%-го раствора КОН плотностью 1,111 г/мл потребуется для взаимодействия с алюминием (с образованием тетрагидроксиалюмината калия), полученным электролизом раствора сульфата алюминия в течение 300 мин при силе тока 25 А?
14. Сколько миллилитров 20%-го раствора серной кислоты плотностью 1,139 г/мл потребуется для взаимодействия с цинком, полученным электролизом раствора сульфата цинка в течение 100 мин при силе тока 55 А?
15. Какой объем оксида азота(IV) (н.у.) получится при взаимодействии избытка горячей концентрированной азотной кислоты с хромом, полученным электролизом раствора сульфата хрома(III) в течение 100 мин при силе тока 75 А?
16. Какой объем оксида азота(II) (н.у.) получится при взаимодействии избытка раствора азотной кислоты с медью, полученной электролизом расплава хлорида меди(II) в течение 50 мин при силе тока 10,5 А?
17. В течение какого времени необходимо проводить электролиз расплава хлорида железа(II) при силе тока 30 А, чтобы получить железо, необходимое для полного взаимодействия со 100 г 30%-го раствора соляной кислоты?
18. В течение какого времени необходимо проводить электролиз раствора нитрата никеля при силе тока 15 А, чтобы получить никель, необходимый для полного взаимодействия с 200 г 35%-го раствора серной кислоты при нагревании?
19. Расплав хлорида натрия подвергли электролизу при силе тока 20 А в течение 30 мин, а расплав хлорида калия подвергли электролизу в течение 80 мин при силе тока 18 А. Оба металла растворили в 1 кг воды. Найдите концентрацию щелочей в полученном растворе.
20.
Магний, полученный электролизом
расплава хлорида магния в течение 200 мин при силе
тока
10 А, растворили в 1,5 л 25%-го раствора серной
кислоты плотностью 1,178 г/мл. Найдите концентрацию
сульфата магния в полученном растворе.
21. Цинк, полученный электролизом раствора сульфата цинка в течение 100 мин при силе тока
17 А, растворили в 1 л 10%-го раствора серной кислоты плотностью 1,066 г/мл. Найдите концентрацию сульфата цинка в полученном растворе.
22. Железо, полученное электролизом расплава хлорида железа(III) в течение 70 мин при силе тока 11 А, превратили в порошок и погрузили в 300 г 18%-го раствора сульфата меди(II). Найдите массу меди, выпавшей в осадок.
23.
Магний, полученный электролизом
расплава хлорида магния в течение 90 мин при силе
тока
17 А, погрузили в раствор соляной кислоты, взятый в
избытке. Найдите объем и количество
выделившегося водорода (н.у.).
24. Раствор сульфата алюминия подвергли электролизу в течение 1 ч при силе тока 20 А. Сколько граммов 15%-го раствора соляной кислоты потребуется для полного взаимодействия с полученным алюминием?
25. Сколько литров кислорода и воздуха (н.у.) потребуется для полного сжигания магния, полученного электролизом расплава хлорида магния в течение 35 мин при силе тока 22 А?
Ответы и решения см. в следующих номерах
Промышленные сорта технически чистого железа (типа Армко), получаемые пирометаллургическим способом, имеют степень чистоты 99,75-99,85%. Дальнейшее удаление содержащихся в этом железе главным образом неметаллических примесей (С, О, S, Р, N) возможно специальной переплавкой в высоком вакууме или отжигом в атмосфере сухого водорода. Однако даже после подобной обработки содержание примесей достигает 2000-1500 частей на миллион частей железа, причем основными примесями являются С, Р, S, Mn и О.
Железо более высокой степени чистоты получают электролитическим и химическим методами, но и оно требует дополнительной сложной очистки.
Электролитическими способами железо получают из умеренно концентрированных или концентрированных растворов хлорида или сульфата железа соответственно при малых плотностях тока и комнатных температурах или высоких плотностях и температурах порядка 100°.
По одному из способов железо осаждали из раствора следующего состава, г/л: 45-60 Fe2+ (в виде FeCl2), 5-10 BaCl2 и 15 NaHCOs. В качестве анодов использовали пластины из армко-железа или уральского кровельного железа, в качестве катодов - чистый алюминий. Электролиз вели при комнатной температуре и плотности тока 0,1 а/дм2. Получали осадок с крупнокристаллической структурой, содержащий около 0,01 % С, следы фосфора и не содержащий серы.
Чистота электролитического железа зависит от чистоты электролита и чистоты металла анодов. При осаждении могут быть удалены примеси более благородные, чем железо, например олово, цинк, медь. He поддаются удалению никель, кобальт, марганец. Общее содержание примесей в электролитическом железе примерно такое же, как и в технически чистом железе. В нем обычно содержится значительное количество кислорода (до 0,1-0 2%), а также серы (0,015-0,05%), если осаждение производилось из сульфатных ванн.
Удаление кислорода из электролитического железа осуществляется восстановительными процессами: обработкой жидкого или твердого металла водородом или раскислением в вакууме расплава углеродом. Отжигом в токе сухого водорода при 900-1400° удается снизить содержание кислорода до 0,003%.
Для получения железа высокой чистоты в полупромышленных масштабах используется способ восстановления водородом в вакуумной плавильной установке. Электролитическое железо сначала подвергается десульфурации присадкой марганца в тигле из извести и плавикового шпата в атмосфере окиси углерода (содержание серы снизилось с 0,01 до 0,004%), затем расплав восстанавливается водородом путем обдувки или продувки в тигле из окиси алюминия. При этом удавалось снизить содержание кислорода до 0,004-0,001%. Десульфурацию металла можно также проводить в высоком вакууме, используя добавки в расплав таких металлов (олово, сурьма, висмут), которые образуют летучие сульфиды. Путем раскисления расплава углеродом в высоко-вакуумных печах удается получить железо с содержанием кислорода и углерода до 0,002% каждого.
Получение железа с более низким содержанием кислорода раскислением в высоком вакууме затруднено взаимодействием металла с материалом тигля, которое сопровождается переходом кислорода в металл. Наилучшим материалом тиглей, обеспечивающим минимальный переход кислорода, являются ZrO2 и ThO2.
Высокочистое железо получают также карбонильным методом из пентакарбонила Fe(CO)5 разложением его при 200-300°. Карбонильное железо не содержит обычно сопутствующих железу примесей - серы, фосфора, меди, марганца, никеля, кобальта, хрома, молибдена, цинка, кремния. Специфическими примесями в нем являются углерод и кислород. Наличие кислорода обусловлено вторичными реакциями между образующейся двуокисью углерода и железом. Содержание углерода достигает 1%; его можно снизить до 0,03%, если к парам карбонила железа добавлять небольшое количество аммиака или обрабатывать порошок железа в водороде. Удаление углерода и кислорода достигается теми же способами вакуумной плавки, которые используются и для электролитического железа.
Наиболее чистое железо может быть получено химическим способом, однако этот способ весьма сложен и дает возможность получить металл в небольших количествах. В химических способах для очистки солей железа от примесей Co, Ni, Cu, Cr, Mn применяют рекристаллизацию, реакции осаждения или извлечения примесей осаждением.
Один из химических методов, позволяющий получить железо весьма высокой степени чистоты (менее 30-60 частей примесей на миллион), включает следующие последовательные стадии:
1) извлечение комплекса FeCl3 эфиром из раствора 6-н HCl с регенерацией водного раствора и последующим извлечением эфира;
2) восстановление FeCls до FeCl2 железом высокой чистоты;
3) дополнительная очистка FeCl2 от меди обработкой сернистым реактивом, а затем эфиром;
4) электролитическое осаждение металла из раствора FeCl2;
5) отжиг зерен металла в водороде (для удаления кислорода и углерода);
6) получение компактного железа методом порошковой металлургии (прессование в прутки и спекание в водороде)
Последняя стадия может быть осуществлена путем бестигельной зонной плавки, которая устраняет недостаток вакуумной обработки - переход кислорода из тигля в металл.
14.06.2019
Гибочный станок для арматуры от Авангард. Принцип работы, особенности конструкции и обзорные данные приспособлений, агрегатов, аппаратов и прочего оборудования для гибки...
14.06.2019
При замене мойки на кухонном пространстве, во время монтажа смесителя, ванны, окон и дверей предусматривается использование герметиков. Это особые композитные вещества,...
13.06.2019
Основным предназначением покрасочной камеры называют высококачественное и равномерное окрашивание транспортного средства. Конечно же, такой метод нельзя назвать...
13.06.2019
Алмалыкское горное металлургическое предприятие приступило к воплощению в жизнь второй стадии программы, направленной на возведение объектов железнодорожной...
13.06.2019
Токарные работы являются одним из типов обработки изделий, в ходе которых стандартная заготовка из металла превращается в нужные конструкционный элемент. Для выполнения...
13.06.2019
С годами в этом мире заметна тенденция к наращиванию производства металлических конструкций. Значительный спрос на подобные сооружения связан с их выгодой в...
12.06.2019
Корпорация из Бразилии Vale сделала заявление по поводу того, что она планирует выделить один миллиард девятьсот миллионов американских долларов на удаление и увеличение...
12.06.2019
Терраса или как её любят называть в народе, веранда, является важнейшим атрибутом любого загородного дома сегодня. Мало кто будет спорить с тем, что она обладает большим...
12.06.2019
В настоящий момент нержавеющий металлический прокат готов предложить потребителям большое количество продукции вроде нержавеющей арматуры, уголков, шестигранников,...
При прохождении электрического тока через металлы (проводники 1-го рода) химические реакции не происходят, и металлы остаются неизменными. Если же электрический ток проходит через расплав или раствор электролита (проводники 2-го рода), на границе электролит - металлический проводник (электрод) происходят различные химические реакции (электролиз) и образуются новые соединения.
Электролизом называется совокупность процессов, происходящих при прохождении электрического тока через электрохимическую систему, состоящую из двух электродов и расплава или раствора электролита.
При электролизе катионы перемещаются к отрицательному электроду (катоду), а анионы - к положительному электроду (аноду). При этом, однако, не всегда катионы и анионы электролита разряжаются, принимая или отдавая электроны. Часто в реакциях электролиза принимает участие растворитель-электролит, например, вода.
Принципиальное различие между реакциями в гальваническом элементе и электролизере заключается только в их направлении и самопроизвольности. В замкнутой цепи гальванического элемента электрохимическая реакция протекает самопроизвольно, а в электролизере - только под воздействием электрического тока внешнего источника.
Следует обратить внимание на название электродов: в гальваническом элементе отрицательный электрод - анод, а положительный - катод; в электролизере, наоборот, отрицательный электрод - катод, а положительный - анод.
При этом следует помнить, что термины «отрицательный» и «положительный» всегда относятся к полюсам источника тока, именно так они и обозначают электроды электролизера. Общее в этих процессах состоит в том, что как в гальваническом элементе, так и в электролизере на отрицательном электроде создается избыток электронов, а на положительном - их недостаток. На катоде ионы или молекулы восстанавливаются под действием электронов, на аноде частицы окисляются, отдавая свои электроны электроду.
В электролизере катионы (М n +) перемещаются к катоду (–), а анионы (А n –) - к аноду (+).
Напряжением разложения электролита при электролизе называется минимальное напряжение (внешняя ЭДС), которое нужно приложить к электродам. Например, для раствора хлорида цинка при стандартных условиях:
Zn 2+ + 2ē = Zn φ° = – 0,76 B,
Cl 2 + 2ē = 2Cl – φ° = + 1,36 В,
и напряжение разложения равно (по абсолютной величине) сумме стандартных электродных потенциалов обоих электродов: 0,76 + 1,36 = 2,12 В, т.е. напряжение разложения не может быть ниже ЭДС соответствующего гальванического элемента.
Напряжение разложения составляется из потенциалов двух электродов - потенциалов разряжения ионов.
Потенциал разряжения катиона иногда называют потенциалом осаждения металла. Это тот минимальный потенциал, который должен быть приложен к электроду для того, чтобы катион потерял заряд и произошло осаждение металла. Для некоторых ионов (Cu 2+ , Ag + , Cd 2+) потенциал осаждения близок к электродному потенциалу, для других же ионов (Fe 2 + , Co 2 + , Ni 2 +) потенциалы осаждения значительно превышают электродные потенциалы металлов - для электролиза необходимо определенное перенапряжение.
Различают электролиз растворов и электролиз расплавов . Электролиз растворов подразделяют на электролиз с инертными электродами и электролиз с растворимым анодом . Инертными могут быть металлические (Pt, Au) и неметаллические (графит) электроды. В качестве растворимых используют аноды из Cr, Ni, Cd, Zn, Ag, Cu и др.
Некоторые металлы практически не растворяются из-за высокой анодной поляризации, например Ni и Fe в щелочном растворе, Pb в H 2 SO 4 .
Электролиз растворов с инертными электродами. При электролизе водных растворов электролитов часто вместо металла на катоде выделяется не металл, а водород. В кислотных средах водород образуется по реакции:
2H + + 2ē = H 2 .
В нейтральных и щелочных средах водород образуется по реакции с участием молекул воды:
2H 2 O + 2ē = H 2 + OH – .
Такие катионы, как Na + или К + , в водном растворе вообще не разряжаются, а выделяется водород.
Катионы могут быть сгруппированы по способности разряжаться в ряд от неразряжающихся до легко разряжающихся. При этом изменяются и продукты электролиза. Для некоторых катионов возможно одновременное образование металла и водорода.
Ниже даны катионы в порядке понижения трудности их разряжения и продукты электролиза:
Катионы Продукты электролиза
Li + , K + , Na + , Mg 2+ , Al 3+ , H + (перенапр.) H 2
Mn 2+ , Zn 2+ , Cr 3 + , Fe 2 + , H + (рН 7) M + H 2
Co 2+ , Ni 2+ , Sr 2+ , Рb 2+ , Н + (рН 0) M + H 2
Cu 2+ , Ag + , Au 3 + M
Различное положение водорода в этом ряду объясняется следующими причинами. Положение водорода между свинцом и медью соответствует численным значениям стандартных электродных потенциалов при С M n + = С H + = 1 моль/л, т.е. при рН=0. Положение водорода между железом и кобальтом соответствует электродному потенциалу водорода в воде при рН=7 (φº H 2 / H + = –0,414 В). При этих условиях из растворов могут быть осаждены все металлы, значение φ° которых больше, чем –0,414 В. Однако на практике кроме кобальта, никеля, олова и свинца удается из водных растворов осадить также цинк, хром и железо. Это объясняется тем, что выделение на катоде газообразного водорода затрудняется перенапряжением водорода.
Таким образом, в ряду катионов от Li + до А1 3+ металл не образуется, а при электролизе выделяется водород за счет восстановления воды. В ряду катионов от Мn 2+ до Рb 2+ при электролизе образуются одновременно металл и водород, и, наконец, в ряду Cu 2+ - Au 3+ образуется только металл .
Следовательно, чем левее (ближе к началу) стоит металл в ряду стандартных электродных потенциалов (ряд напряжений), тем труднее выделить этот металл электролизом водного раствора.
Если к раствору, содержащему несколько катионов, приложить постепенно возрастающее напряжение, то электролиз начинается тогда, когда достигается потенциал осаждения катиона с самым высоким электродным потенциалом (наиболее положительным). При электролизе раствора, содержащего ионы цинка (φ°= –0,76 В) и меди (φ° = +0,34 В), на катоде вначале выделяется медь, и лишь после того, как почти все ионы Сu 2+ разрядятся, начнет выделяться цинк. Таким образом, если в растворе одновременно содержатся различные катионы, то при электролизе их можно выделить последовательно в соответствии со значениями их электродных потенциалов . При этом предполагается, что перенапряжение выделения металлов для них примерно одинаково (и невелико).
Что касается потенциалов разряжения анионов , то здесь картина намного сложнее из-за способности воды участвовать в процессе электролиза. В общем случае можно сказать, что на аноде сначала разряжаются анионы с самым низким потенциалом (наименее положительные). Если раствор содержит ионы Сl – (φº=1,36 В), Вr – (φ° = 1,09 В) и I – (φº = 0,54 В), то сначала будет образовываться йод, затем бром и, наконец, хлор. Фторид-ионы в водном растворе вообще разряжаться не могут (φ° = 2,87 В).
Большинство кислородсодержащих анионов (кроме ацетат-иона) в водном растворе не разряжаются, вместо них в кислотных и нейтральных растворах происходит разложение воды:
2Н 2 О – 4ē = О 2 + 4Н + ,
а в щелочных растворах - разрядка гидроксид-ионов:
2OH – – 2 ē = 1 / 2 O 2 + H 2 O.
Анионы по их способности разряжаться при электролизе водных растворов располагаются в следующем ряду от неразряжающихся в водном растворе анионов кислородсодержащих кислот типа SO 4 2– , NO 3 – до легкоразряжающихся:
Анионы Продукты электролиза
SO 4 2– , NO 3 – и т. п., ОН – O 2
Сl – , Вr – , I – Cl 2 (ClO – , ClO 3 –), Br 2 , I 2 (+O 2)
S 2– S, SO 2 (+ O 2)
Таким образом, можно сформулировать следующие основные правила электролиза водных растворов электролитов с нерастворимыми электродами :
1. Из анионов электролитов в первую очередь разряжаются на аноде анионы бескислородных кислот (Cl – , Br – , S 2– и т.д.).
2. Анионы кислородсодержащих кислот (SO 4 2– , NO 3 – , CO 3 2– и т.д.) в присутствии воды не разряжаются, вместо них окисляется вода по реакции:
2H 2 O – 4ē = O 2 + 4H + .
3. Активные металлы, расположенные в ряду напряжений до Al (включительно) на катоде не восстанавливаются, вместо них восстанавливается вода:
2H 2 O + 2ē = H 2 + 2OH – .
4. Металлы, расположенные в ряду напряжений после алюминия, но до водорода, восстанавливаются на катоде наравне с молекулами воды:
К: 1) Zn 2+ + 2ē = Zn
2) 2H 2 O + 2ē = H 2 + 2OH – .
5. Металлы, имеющие положительное значение электродного потенциала восстанавливаются на катоде в первую очередь:
Cu 2+ + 2ē = Cu
Например, при электролизе серной кислоты (графитовые электроды) происходят следующие процессы:
на катоде 2Н + + 2ē = Н 2 ,
на аноде 2Н 2 О – 4ē = О 2 + Н + .
Суммарное уравнение:
2H 2 O = 2H 2 + O 2 ,
т.е. при электролизе раствора серной кислоты водород и кислород выделяются за счет разложения молекул воды. Продукты электролиза: водород и кислород.
Электролиз раствора сульфата меди:
на катоде Сu 2 + + 2ē = Сu,
на аноде 2Н 2 О – 4ē = O 2 + 4H +
Суммарное уравнение:
2Cu 2+ + 2H 2 O = 2Cu + O 2 + 4H +
2CuSO 4 + 2Н 2 О = 2Сu + О 2 + 2H 2 SO 4 .
Продукты электролиза: медь, кислород, серная кислота.
Возможность разряжения аниона зависит от его концентрации. Так, продукты электролиза концентрированного и разбавленного растворов NaCl - хлор и кислород соответственно.
Электролиз разбавленного раствора хлорида натрия проходит без разряжения ионов Сl – (и соответственно ионов Na +), т.е. происходит разложение воды. По мере повышения концентрации соли на аноде вместе с кислородом начинается выделение хлора, и в концентрированных растворах образуется хлор (с примесью кислорода):
на катоде 2H 2 O + 2ē = H 2 + 2OH –
на аноде 2Сl – – 2ē = Cl 2 .
Суммарное уравнение:
2Cl – + 2H 2 O = H 2 + Cl 2 + 2OH –
2NaCl + 2H 2 O = H 2 + Cl 2 + 2NaOH.
Продукты электролиза: водород, хлор и гидроксид натрия.
В случае выделения хлора при электролизе растворов хлоридов на основной процесс образования хлора накладываются реакции взаимодействия хлора с водой (гидролиз) и последующих превращений образующихся веществ. Гидролиз хлора проходит с образованием слабой хлорноватистой кислоты и хлорид-ионов (соляная кислота):
Сl 2 + Н 2 О = Н + + Сl – + НС1О.
Хлорноватистая кислота с образующейся при электролизе щелочью (точнее, Na + +OH –) дает в качестве продукта гипохлорит натрия NaClO. В щелочной среде суммарное уравнение реакции имеет вид:
Сl 2 + 2NaOH = NaCl + NaClO + Н 2 О.
При повышенных температурах (кипение воды) гидролиз хлора проходит с образованием хлорат-иона. Возможные уравнения реакций:
3Cl 2 + 3H 2 O = ClO 3 – + 5 Cl – + 6H + ,
3НСlO = СlO 3 – + 2Сl – + 3Н + ,
3СlО – = СlO 3 – + 2Сl – .
В щелочной среде суммарное уравнение имеет вид
3Сl 2 + 6NaOH = NaClO 3 + 5NaCl + 3Н 2 О.
Электролиз с диафрагмой. При электролизе разбавленного раствора хлорида натрия к катоду перемещаются ионы Na + , но выделяется водород:
2Н 2 О+2ē = Н 2 + ОН –
и концентрируется раствор гидроксида натрия.
К аноду перемещаются хлорид-ионы, но из-за их низкой концентрации в основном образуется не хлор, а кислород:
2H 2 O – 4ē = O 2 + 4H +
и концентрируется раствор соляной кислоты.
Если электролиз проводится в химическом стакане или другом подобном сосуде, растворы щелочи и кислоты смешиваются и электролиз сводится к образованию водорода и кислорода за счет разложения воды. Если же анодное и катодное пространства разделить перегородкой (диафрагмой), пропускающей ионы-переносчики тока, но препятствующей смешению приэлектродных растворов, то можно в качестве продуктов электролиза получить растворы кислоты и щелочи.
При электролизе раствора хлорида натрия гидроксид-ионы, образовавшиеся на катоде по реакции:
2H 2 O + 2ē = H 2 + 2OH –
сразу же начинают участвовать в переносе электричества и вместе с ионами С1 – перемещаются к аноду, где оба иона разряжаются и образуется смесь кислорода и хлора. Поэтому выход хлора падает. Если анод изготовлен из угля (графита), то он окисляется кислородом и образуются оксиды углерода СО и СО 2 , загрязняющие хлор. Далее хлор, образующийся на аноде, взаимодействует с гидроксид-ионами:
С1 2 + ОН – = Н + + Сl – + ОСl – .
Образование гипохлорит-ионов - также нежелательный процесс (если получение раствора гипохлорита натрия не является целью). Всех этих нежелательных последствий удается избежать, если пользоваться диафрагмой, разделяющей катодное и анодное пространства и задерживающей ионы ОН – , но пропускающей ионы Сl – . Наконец, диафрагма препятствует диффузии газов и позволяет получить более чистый водород.
Если в растворе содержится несколько анионов, предсказать последовательность их разряжения на аноде сложнее, чем катионов, но, вообще говоря, соблюдается правило, что в первую очередь разряжается анион, характеризующийся самым низким значением потенциала (или самым высоким отрицательным значением электродного потенциала реакции, проходящей на аноде).
Электролиз растворов с растворимым анодом. Электролиз с растворимым анодом возможен тогда, когда металл легче отдает электроны, чем ионы Сl – , ОН – или молекулы воды. Например, на медном аноде в растворе хлорида или сульфата меди хлор или кислород не выделяются, а происходит переход в раствор ионов Сu 2+ . Одновременно на катоде те же ионы разряжаются и осаждается металлическая медь. Таким образом, электролиз с растворимым анодом сводится к переносу меди с анода на катод.
Реакция на аноде в большинстве случаев усложняется многочисленными побочными и часто нежелательными процессами. Например, образующиеся ионы могут образовывать оксиды, гидроксиды и их пленки:
М 2+ + 2ОН – = МО + Н 2 О.
На аноде возможно также выделение кислорода:
2H 2 O – 4ē = O 2 + 4H + ,
который может участвовать в самых различных реакциях электролитической системы.
При образовании газообразных продуктов, особенно кислорода, в большинстве случаев потенциалы разложения не соответствуют электродным потенциалам из-за высоких значений перенапряжения. Перенапряжением называют разность между реальным напряжением разложения и теоретически рассчитанным из электродных потенциалов ЭДС соответствующей реакции . Особенно сильно влияют на величину перенапряжения природа выделяющегося вещества (для хлора, брома и йода перенапряжение очень незначительно) и материал электрода. Ниже приведены данные по перенапряжению при выделении водорода и кислорода на различных катодах и анодах.
Электрод Перенапряжение, В
Водород Кислород
Pt черненая 0,00 0,2–0,3
Pt блестящая 0,1 0,4–0,5
Fe 0.1–0,2 0,2–0,3
Ni 0,1–0,2 0,1–0,3
Сu 0,2 0,2–0,3
Pb 0,4–0,6 0,2–0,3
Перенапряжение зависит также от формы электродов, состояния их поверхности, плотности тока, температуры раствора, интенсивности перемешивания раствора и других факторов.
Перенапряжение водорода на железе равно ~ 0,1 В, а кислорода на том же материале ~ 0,3 В. Следовательно, перенапряжение при электролизе на железных электродах составит 0,1 + 0,3 = 0,4 В. Сумма этого значения и теоретически вычисленного составит минимальное значение напряжения разряжения соответствующего электролита.
Отношение к перенапряжению - двойственное. С одной стороны, перенапряжение приводит к повышенному расходу электроэнергии, с другой стороны, благодаря перенапряжению удается осаждать из водных растворов многие металлы, которые по значениям их стандартных электродных потенциалов осаждаться не должны. Это Fe, Pb, Sn, Ni, Co, Zn, Cr. Именно благодаря перенапряжению, а также влиянию концентрации раствора на электродный потенциал возможны электролитическое хромирование и никелирование железных изделий, а на ртутном электроде удается получить из водного раствора даже натрий.
Разряжение в водном растворе ионов Сl – , а не ОН – в растворах с высокой концентрацией электролита также объясняется перенапряжением кислорода. Однако этого перенапряжения оказывается недостаточно, чтобы произошло разряжение ионов F – и выделение свободного фтора.
На величину перенапряжения влияют многие другие кинетические факторы - скорости переноса частиц к электродам и отвода продуктов электролиза, скорость процесса разрушения гидратных и других оболочек разряжающихся ионов, скорость соединения атомов в двухатомные газовые молекулы и т. п.
Вариант 1
1.Напишите уравнения реакций: а) получения цинка из оксида цинка путем восстановления углём; б) получения кобальта из оксида кобальта (II) путем восстановления водородом; в) получения титана из хлорида титана (IV) магний термическим способом. Реакцию в разберите как окислительно-восстановительную: обозначьте степени окисления атомов и расставьте коэффициенты, определив их методом электронного баланса.
2.Составьте схемы и уравнения реакций, протекающих при электролизе: а) расплава хлорида калия; б) раствора бромида цинка; в) раствора сульфата железа (II).
3.В чем заключается сущность коррозии металлов? Какие виды коррозии вам известны?
Коррозия – это самопроизвольное разрушение металлов и сплавов в результате химического, электрохимического или физико-химического взаимодействия с окружающей средой.
4.На стальной крышке поставлена медная заклёпка. Что раньше разрушится – крышка или заклёпка? Почему?
Стальная крышка, поскольку она включает в себя железо, а железо более активный металл, чем медь и будет скорее коррозировать. Также железо с медью образуют гальваническую пару, где железо – анод, и разрушается скорее, в медь – катод, остается нетронутым.
Вариант 2
1.Напишите уравнения реакций: а) получения железа из оксида железа (III) алюминотермическим способом; б) получения меди из оксида меди (II) путём восстановления углём; в) получения вольфрама из его высшего оксида путем восстановления водородом. Реакцию в разберите как окислительно-восстановительную: обозначьте степени окисления атомов и расставьте коэффициенты, определив их методом электронного баланса.
2.Составьте схемы и уравнения реакций, протекающих при электролизе: а) раствора бромида меди (II); б) раствора иодида натрия; в) раствора нитрата свинца (II).
3.Какие факторы приводят к усилению коррозии металлов?
4.Почему лужённый (покрытый оловом) железный бак на месте повреждения защитного слоя быстро разрушается?
Также железо с оловом образуют гальванический элемент, где железо – анод, и разрушается скорее, а олово – катод, остается нетронутым.
Вариант 3
1.Напишите уравнения реакций: а)получения меди из оксида меди (II) путём восстановления водородом; б) получения железа из оксида железа (III) путем восстановления оксидом углерода (II); в) получения ванадия из оксида ванадия (V) кальцийтермическим способом. Реакцию в разберите как окислительно-восстановительную: обозначьте степени окисления атомов и расставьте коэффициенты, определив их методом электронного баланса.
2.Составьте схемы и уравнения реакций, протекающих при электролизе: а) расплава хлорида кальция; б) раствора бромида калия; в) раствора сульфата цинка.
3.Какие факторы способствуют замедлению коррозии металлов?
-Нейтрализация или обескислороживание коррозионных сред, а также применение различного рода ингибиторов коррозии;
-Устранения из металла или сплава примесей, ускоряющих коррозионный процесс (устранение железа из магниевых или алюминиевых сплавов, серы из железных сплавов).
-Исключение неблагоприятных металлических контактов или их изоляция, устранение щелей и зазоров в конструкции, устранение зон застоя влаги.
4. Какие металлы при взаимном контакте в присутствии электролита быстрее разрушаются: а) медь и цинк; б) алюминий и железо? Почему?
Быстрее разрушаться будет более активный металл из данной пары
а) цинк более активный металл, чем медь;
б) алюминий более активный металл, чем железо.
Вариант 4
1.Напишите уравнения реакций: а)получения молибдена из его высшего оксида путем восстановления водородом; б)получения хрома из оксида хрома (III) алюминотермическим способом; в) получения никеля из оксида никеля (II) путем восстановления углем. Реакцию в разберите как окислительно-восстановительную: обозначьте степени окисления атомов и расставьте коэффициенты, определив их методом электронного баланса.
2.Составьте схемы и уравнения реакций, протекающих при электролизе: а)раствора хлорида меди (II); б) раствора иодида натрия; в) раствора нитрата никеля (II).
3.Перечислите способы борьбы с коррозией металлов.
4.Почему на оцинкованном баке на месте царапины цинк разрушается, а железо не ржавеет?
Цинк более активный металл, чем железо. Также железо с цинком образуют гальванический элемент, где цинк – анод, и разрушается скорее, а железо – катод, остается нетронутым.





